清華大學(xué)生命學(xué)院高寧研究組與香港科技大學(xué)戴碧瓘研究組
共同在《自然》發(fā)文揭示真核生物DNA復(fù)制解旋酶高分辨三維結(jié)構(gòu)
清華新聞網(wǎng)7月31日電 7月29日,清華大學(xué)高寧研究組和香港科技大學(xué)戴碧瓘教授研究組共同在《自然》(Nature)雜志上以長文形式在線發(fā)表了題為《真核生物DNA復(fù)制解旋酶MCM復(fù)合物的3.8埃分辨率結(jié)構(gòu)》(Structure of the Eukaryotic Minichromosome Maintenance Complex at 3.8 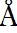 )的研究論文,首次報(bào)道了真核生物DNA復(fù)制起始與延伸過程中DNA解旋酶核心組分MCM2-7復(fù)合物的3.8 埃高分辨率冷凍電鏡結(jié)構(gòu),并以此為基礎(chǔ)對(duì)DNA復(fù)制起始時(shí)MCM2-7復(fù)合物的作用機(jī)理進(jìn)行了分析。
)的研究論文,首次報(bào)道了真核生物DNA復(fù)制起始與延伸過程中DNA解旋酶核心組分MCM2-7復(fù)合物的3.8 埃高分辨率冷凍電鏡結(jié)構(gòu),并以此為基礎(chǔ)對(duì)DNA復(fù)制起始時(shí)MCM2-7復(fù)合物的作用機(jī)理進(jìn)行了分析。
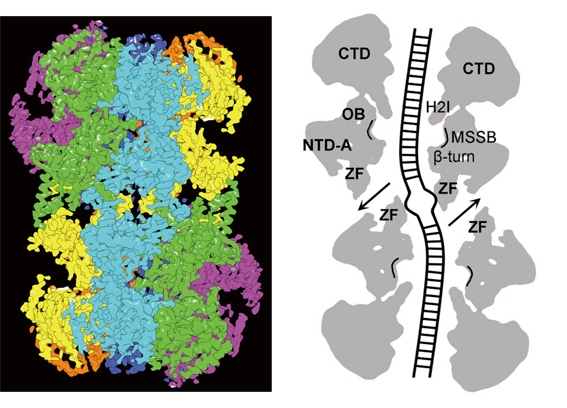
MCM2-7雙六聚體復(fù)合物高分辨率冷凍電鏡結(jié)構(gòu)及中央孔道結(jié)構(gòu)示意圖。梯狀為雙鏈DNA。
該論文是清華大學(xué)國家蛋白質(zhì)基礎(chǔ)設(shè)施(北京)建立以來,完全利用此平臺(tái)進(jìn)行數(shù)據(jù)收集及處理而發(fā)表的首篇世界頂級(jí)雜志科研論文。《自然》雜志同期刊發(fā)了“News & Views”評(píng)論文章重點(diǎn)推薦介紹了這項(xiàng)工作。來自美國匹茲堡大學(xué)的DNA復(fù)制領(lǐng)域的著名生化學(xué)家Schwacha教授指出這項(xiàng)工作的重要之處在于“揭示了DNA復(fù)制過程的一個(gè)關(guān)鍵步驟——雙鏈DNA的初始解鏈——是如何發(fā)生的”。
遺傳信息載體DNA在細(xì)胞內(nèi)的復(fù)制受到嚴(yán)格的調(diào)控。雙鏈DNA的復(fù)制包括解旋和復(fù)制兩個(gè)過程,復(fù)制起始的一個(gè)關(guān)鍵步驟是DNA解旋酶的結(jié)合和激活。MCM2-7復(fù)合物負(fù)責(zé)在DNA復(fù)制起始和延伸階段進(jìn)行雙鏈DNA的解螺旋。DNA復(fù)制異常會(huì)導(dǎo)致基因組的不穩(wěn)定,與多種人類惡性腫瘤的發(fā)生、發(fā)展具有密切的關(guān)系;作為DNA復(fù)制解旋酶的核心組分,MCM2-7本身的基因突變或異常表達(dá)也與很多人類疾病密切相關(guān)。例如,MCM4基因的突變可以導(dǎo)致小鼠乳腺癌的發(fā)生。
由于MCM2-7復(fù)合物功能機(jī)制的重要性,在過去三十年里,相關(guān)領(lǐng)域研究人員對(duì)其進(jìn)行了大量的功能和結(jié)構(gòu)方面的研究。由于其結(jié)構(gòu)的復(fù)雜性,針對(duì)MCM2-7復(fù)合物的高分辨三維結(jié)構(gòu)解析一直停滯不前,已成為其功能研究的重要限制因素。2013年下半年開始,高寧研究組和香港科技大學(xué)戴碧瓘研究組合作,利用清華大學(xué)冷凍電鏡平臺(tái)對(duì)MCM2-7雙六聚體復(fù)合物以及與相關(guān)功能因子結(jié)合的復(fù)合物進(jìn)行結(jié)構(gòu)解析。初期主要是利用負(fù)染電鏡和冷凍電鏡的方法對(duì)相關(guān)復(fù)合物進(jìn)行分析。2014年下半年,Titan Krios電鏡更換新一代的K2相機(jī)后,在之前條件優(yōu)化的基礎(chǔ)上,該課題獲得了關(guān)鍵性突破,進(jìn)而解析來自酵母菌分裂間期G1期MCM2-7雙六聚體復(fù)合物近原子分辨率的三維結(jié)構(gòu)。結(jié)構(gòu)分析表明,兩個(gè)MCM2-7單六聚體呈二次對(duì)稱,并相對(duì)于中心軸線有一定角度的傾斜和扭轉(zhuǎn),在中心形成一個(gè)扭曲的中央通道。四層結(jié)構(gòu)域組成的環(huán)狀結(jié)構(gòu)限制了中央通道的大小,使之具有了完美匹配雙螺旋DNA的直徑(圖)。這些結(jié)構(gòu)分析表明MCM2-7復(fù)合物直接參與了復(fù)制起始時(shí)的DNA最初解鏈過程。這一高分辨率的結(jié)構(gòu)為真核生物特異的解旋酶家族蛋白復(fù)合物的組裝、激活和調(diào)控的研究提供了一個(gè)全新視點(diǎn),為指導(dǎo)此復(fù)合物的功能研究奠定了良好的基礎(chǔ)。
清華大學(xué)生命學(xué)院2010級(jí)博士生李寧寧(2015年7月已畢業(yè))和香港科技大學(xué)的翟元梁研究助理教授為該論文的共同第一作者。高寧研究員、香港科技大學(xué)的戴碧瓘教授及翟元梁助理教授為共同通訊作者。生命學(xué)院的楊茂君教授參與了原子模型的搭建工作,冷凍電鏡平臺(tái)的總管雷建林博士、2010級(jí)博士生張一小(2015年7月已畢業(yè))和2012級(jí)博士生李婉秋參與了冷凍電鏡數(shù)據(jù)收集工作。論文還得到了生命學(xué)院王佳偉研究員和李雪明研究員在數(shù)據(jù)處理及分析等方面的建議和協(xié)助。該研究獲得了科技部、國家自然科學(xué)基金委、香港研究資助局以及香港科技大學(xué)的經(jīng)費(fèi)支持。
高寧研究員2008年底加入清華大學(xué)生命科學(xué)學(xué)院,2009-2010期間主要參與生命學(xué)院冷凍電鏡實(shí)驗(yàn)平臺(tái)的搭建,一直致力于利用冷凍電鏡三維重構(gòu)技術(shù)研究蛋白質(zhì)的生物合成、降解和核糖體的組裝成熟、蛋白翻譯的調(diào)控等重要生物過程,取得了一系列重要研究成果。先后在《Nature Structural &Molecular Biology》(2014),《PloS Biology》(2014),《Protein & Cell》(2014),《Nucleic Acids Research》(2013, 2013, 2014),《J Biol Chem》(2013)及《PNAS》(2011)等雜志發(fā)表多篇通訊作者研究論文,闡述了蛋白生物合成和降解中的多種調(diào)控機(jī)制。由于高寧研究員近年來的系統(tǒng)性研究成果,先后獲得了多項(xiàng)人才基金(自然基金委優(yōu)秀青年基金2014、北京市青年英才計(jì)劃2013等),以及自然基金委面上項(xiàng)目和科技部重大研究計(jì)劃的支持。
文章鏈接:http://www.nature.com/nature/journal/vaop/ncurrent/full/nature14685.html
評(píng)論文章:http://www.nature.com/nature/journal/vaop/ncurrent/full/nature14643.html
供稿:生命學(xué)院 編輯:襄樺
