清華大學(xué)顏寧研究組在《自然》發(fā)表論文
揭示葡萄糖轉(zhuǎn)運(yùn)蛋白GLUT3識別和轉(zhuǎn)運(yùn)底物的分子機(jī)制
清華新聞網(wǎng)7月16日電 7月15日,清華大學(xué)醫(yī)學(xué)院顏寧研究組在《自然》(Nature)在線發(fā)表題為《葡萄糖轉(zhuǎn)運(yùn)蛋白識別與轉(zhuǎn)運(yùn)底物的分子基礎(chǔ)》(Molecular Basis of ligand recognition and transport by glucose transporters)的長文(Article),報道了人源葡萄糖轉(zhuǎn)運(yùn)蛋白GLUT3處于不同構(gòu)象的3個高分辨率晶體結(jié)構(gòu),并通過與之前該組解析的GLUT1的結(jié)構(gòu)比對,完整揭示了葡萄糖轉(zhuǎn)運(yùn)蛋白底物識別與轉(zhuǎn)運(yùn)的分子機(jī)理,為基于結(jié)構(gòu)的小分子設(shè)計提供了直接依據(jù)。生命科學(xué)聯(lián)合中心博士后(醫(yī)學(xué)院)鄧東和一年級博士生(生命學(xué)院)孫鵬程為本文的共同第一作者,顏寧教授為本文的通訊作者。
這是顏寧研究組繼7月10日在《科學(xué)》(Science)發(fā)表題為《分枝桿菌Insig同源蛋白晶體結(jié)構(gòu)揭示Insig蛋白感受固醇的分子機(jī)制》(Crystal structure of a mycobacterial Insig homolog provides insight into how these sensors monitor sterol levels)的研究論文之后近期又一篇在頂級期刊發(fā)表的論文。
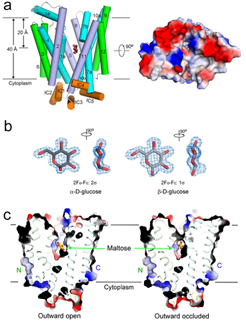
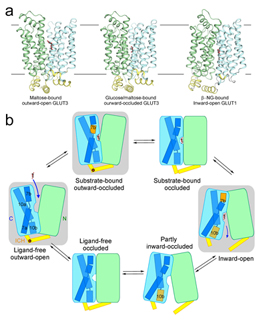
(左圖)人源葡萄糖轉(zhuǎn)運(yùn)蛋白GLUT3處于不同狀態(tài)的3個晶體結(jié)構(gòu)。
(右圖)迄今已獲得的葡萄糖轉(zhuǎn)運(yùn)蛋白GLUTs的晶體結(jié)構(gòu)以及在此基礎(chǔ)上進(jìn)一步完善的GLUTs工作模型。
葡萄糖是地球上各種生物最主要的能源物質(zhì),為生長代謝提供能量,并且作為前體參與合成其他生命組成大分子。葡萄糖分子高度親水,無法自由通過疏水的生物膜,其進(jìn)出細(xì)胞需要依靠膜上的轉(zhuǎn)運(yùn)蛋白完成。主要協(xié)同轉(zhuǎn)運(yùn)蛋白超家族(Major Facilitator Superfamily, MFS)葡萄糖轉(zhuǎn)運(yùn)蛋白GLUTs在此過程中至關(guān)重要。人體中的GLUTs共有14種,目前研究較清楚的是GLUT1,2,3,4(簡稱GLUT1-4),它們負(fù)責(zé)向人體的不同組織轉(zhuǎn)運(yùn)葡萄糖,比如GLUT1主要負(fù)責(zé)葡萄糖進(jìn)入紅細(xì)胞和跨越血腦屏障,GLUT2主要在肝、脾、小腸等內(nèi)臟細(xì)胞中發(fā)揮作用,GLUT3負(fù)責(zé)為神經(jīng)系統(tǒng)攝取葡萄糖,GLUT4則是肌肉和脂肪組織的主要葡萄糖轉(zhuǎn)運(yùn)蛋白。此外,越來越多的研究發(fā)現(xiàn)GLUT1和GLUT3在多種實體瘤中超量表達(dá)。這是由于腫瘤細(xì)胞的快速增殖使其處于缺氧環(huán)境中,無氧條件下依靠糖酵解產(chǎn)生的ATP比有氧代謝少了10倍以上,因此腫瘤細(xì)胞需要大量表達(dá)GLUTs以滿足葡萄糖的超量攝入,這就是被稱為“沃伯格效應(yīng)”(“Warburg effect”)的現(xiàn)象。這一現(xiàn)象使得GLUT1和GLUT3成為了潛在的腫瘤細(xì)胞標(biāo)志物,具有診斷價值。臨床上利用“正電子發(fā)射斷層掃描”(PET)監(jiān)控氟代脫氧葡萄糖(FDG)在人體組織中的分布以監(jiān)控葡萄糖代謝和腫瘤成像,F(xiàn)DG也是通過GLUTs進(jìn)入細(xì)胞。此外,前期實驗顯示一些GLUT1轉(zhuǎn)運(yùn)抑制劑在抑制小鼠腫瘤生長方面表現(xiàn)出較好的效果,使得GLUTs成為了潛在的腫瘤治療靶點。因此,GLUTs的結(jié)構(gòu)生物學(xué)及生物化學(xué)研究將為這一潛在應(yīng)用提供重要的分子基礎(chǔ)。
顏寧教授領(lǐng)導(dǎo)的研究組過去8年致力于系統(tǒng)揭示GLUTs的結(jié)構(gòu)與工作機(jī)理。2012年,她領(lǐng)導(dǎo)的團(tuán)隊解析了GLUTs大腸桿菌同源蛋白XylE與底物分子木糖及抑制劑葡萄糖的復(fù)合物晶體結(jié)構(gòu),并通過同源建模首次描繪出GLUTs的大致結(jié)構(gòu),為研究GLUTs的轉(zhuǎn)運(yùn)機(jī)理研究提供了重要線索(http://www.nature.com/nature/journal/v490/n7420/abs/nature11524.html)。自此以后,她們聚焦于極富挑戰(zhàn)性的人源葡萄糖轉(zhuǎn)運(yùn)蛋白GLUT1-4的結(jié)構(gòu)生物學(xué)研究,并于2014年初解析了具有近一個世紀(jì)研究歷史、備受關(guān)注的人源GLUT1的三維結(jié)構(gòu)(http://www.nature.com/nature/journal/v510/n7503/full/nature13306.html),這也是第一個人源次級轉(zhuǎn)運(yùn)蛋白的晶體結(jié)構(gòu)。
GLUT1的結(jié)構(gòu)處于向胞內(nèi)開放的狀態(tài),是GLUTs蛋白在行使轉(zhuǎn)運(yùn)功能過程中眾多構(gòu)象的一種。為了揭示整個轉(zhuǎn)運(yùn)過程,獲得GLUTs處于其他不同轉(zhuǎn)運(yùn)狀態(tài)下的結(jié)構(gòu)信息至關(guān)重要;為了理解底物識別,則需要獲得GLUTs與底物的復(fù)合物結(jié)構(gòu)。針對這些問題,該研究組精心設(shè)計實驗,利用膜蛋白脂立方相(Lipidic Cubic Phase, LCP)結(jié)晶和微聚焦X-射線衍射,最終解析了人源葡萄糖轉(zhuǎn)運(yùn)蛋白GLUT3處于3種不同狀態(tài)的高分辨率晶體結(jié)構(gòu)。其中GLUT3與底物分子葡萄糖的復(fù)合物晶體結(jié)構(gòu)處于朝向胞外閉合的狀態(tài),分辨率高達(dá)1.5埃,是目前為止分辨率最高的轉(zhuǎn)運(yùn)蛋白結(jié)構(gòu)。這一超高分辨率首次清晰表明GLUT3可以識別葡萄糖α和β兩種異構(gòu)體。
為了進(jìn)一步得到GLUT3蛋白向胞外開放的構(gòu)象,他們推測加入競爭性抑制分子麥芽糖或者纖維二糖之后,可能將GLUT3穩(wěn)定于面向胞外的構(gòu)象,這一猜測獲得生化實驗的支持。最終他們獲得了GLUT3與麥芽糖結(jié)合的向胞外開放和向胞外閉合兩種狀態(tài)下的晶體結(jié)構(gòu)。至此,通過進(jìn)一步比較GLUT1向胞內(nèi)開放的結(jié)構(gòu),GLUT家族蛋白通過交替開放(alternating access)轉(zhuǎn)運(yùn)底物的整個過程已經(jīng)基本呈現(xiàn)在眼前。這不但是對于GLUTs家族轉(zhuǎn)運(yùn)機(jī)制研究的突破性進(jìn)展,也為轉(zhuǎn)運(yùn)蛋白領(lǐng)域和膜蛋白結(jié)構(gòu)生物學(xué)領(lǐng)域的研究起到了導(dǎo)向作用。同時,高分辨率GLUT3與底物結(jié)合的結(jié)構(gòu)也為今后的小分子抑制劑的設(shè)計提供了重要的理論基礎(chǔ)。
此項研究工作得到科技部重大研究計劃的資助。顏寧是清華大學(xué)拜耳講席教授,并獲得美國HHMI國際青年科學(xué)家、杰出青年基金和中組部首批青年拔尖創(chuàng)新人才計劃的支持。
供稿:醫(yī)學(xué)院 生命學(xué)院 編輯:襄樺 田心
