清華新聞網3月8日電 近日,清華大學藥學院胡澤平研究員團隊與合作者共同研究發(fā)文,揭示了胃癌患者血漿的代謝重編程圖譜,發(fā)現(xiàn)基于代謝組學構建的機器學習模型能準確診斷胃癌患者,并預測患者預后風險。
胃癌是東亞地區(qū)高發(fā)的致死性腫瘤。胃癌的早期確診和及時干預對改善臨床結果至關重要。然而,作為胃癌診斷金標準的內鏡活檢因其侵入性高且費用昂貴而限制了臨床應用。因此,迫切需要開發(fā)具有高靈敏度和特異性的新型非侵入性胃癌檢測方法。此外,對病人進行預后監(jiān)測并及時進行干預有助于更好的臨床結果。因此,開發(fā)一種更精確的患者預后預測方法至關重要。
胃作為具有高度異質性的消化器官,其癌變和進展受到基因突變和環(huán)境擾動的雙重影響,伴隨顯著的代謝重塑。然而,代謝重編程及其在胃癌診療中的潛在應用并未被系統(tǒng)性深入地研究過,未能滿足臨床對胃癌早診和患者分層治療的需求。目前的胃癌生物標志物研究很大程度上受限于隊列規(guī)模小、缺乏獨立的驗證隊列、樣本類型和檢測方法的差異導致的結果再現(xiàn)性低,以及受分析技術限制的檢測靈敏度有待提高等問題。因此,使用多中心、大隊列、特征明確的胃癌和對照人群進行代謝組學分析對于識別和驗證具有轉化潛力的生物標志物,從而開發(fā)和完善適合臨床應用的代謝生物標志物仍然勢在必行。
研究人員收集了702例胃癌患者和非胃癌對照的血漿樣本,進行了靶向代謝組學數(shù)據(jù)分析。結果顯示,胃癌患者血漿發(fā)生了明顯的代謝重編程,其中最顯著改變的代謝通路為谷胱甘肽代謝。通路中的兩種關鍵代謝物還原型谷胱甘肽GSH和氧化型谷胱甘肽GSSG在胃癌血漿中顯著降低。此外,作為氧化應激紊亂指示物的GSH/GSSG比率在胃癌患者中顯著上調,并隨著疾病進展而逐漸增加,表明胃癌患者血漿中氧化應激嚴重失調。此外,胃癌患者的半胱氨酸和蛋氨酸代謝通路也發(fā)生顯著失調。與非胃癌對照相比,胃癌患者的S-腺苷-L-同型半胱氨酸 (SAH) 下調,S-腺苷甲硫氨酸 (SAM) 上調,并且SAM/SAH比值隨疾病進展而增加。作為通用甲基供體,SAM豐度和SAM/SAH比值的失調可能反映了胃癌患者甲基池的擾動。這些胃癌血漿中的代謝重編程特征為開發(fā)胃癌檢測和患者預后預測生物標志物奠定了基礎。
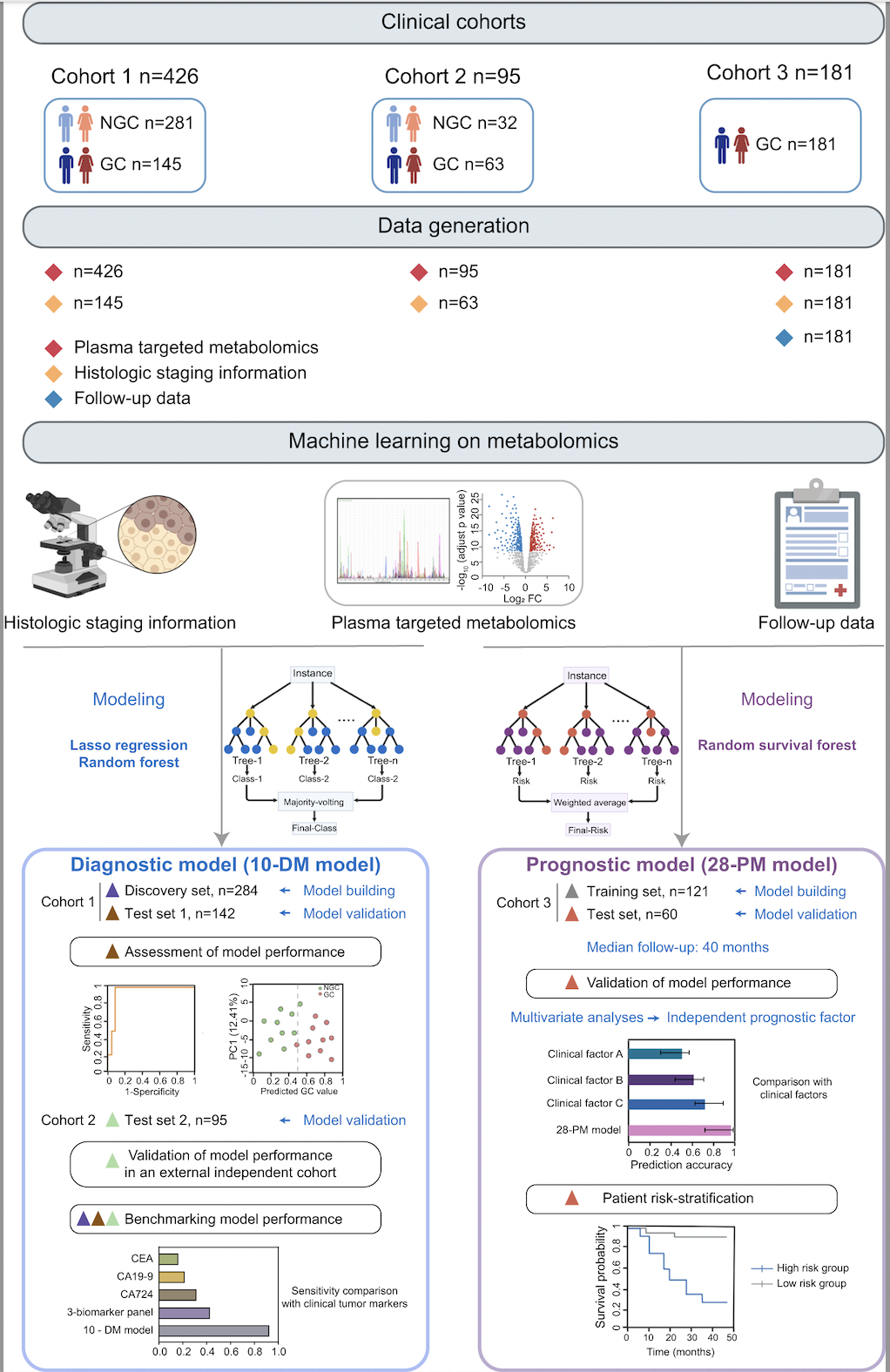
研究設計及流程圖
盡管代謝組學在全面分析胃癌整體代謝特征方面具有獨特的優(yōu)勢,能夠大規(guī)模識別用于GC診斷和預后的有希望的生物標志物,但復雜的組學數(shù)據(jù)的解釋始終是一個挑戰(zhàn)。在過去的幾年中,機器學習算法已被用于發(fā)現(xiàn)組學數(shù)據(jù)和疾病狀態(tài)之間的潛在關聯(lián)并創(chuàng)建預測模型。因此,研究人員分別使用隨機森林和隨機生存森林算法建立了基于10個代謝物的胃癌診斷模型(10-DM)和基于28個代謝物的胃癌患者預后預測模型(28-PM)并在測試集中驗證了模型的優(yōu)越性能。對模型效果評估時發(fā)現(xiàn),10-DM診斷模型即使對早期胃癌患者(stage IA)也能準確診斷,表現(xiàn)出比臨床正在使用的癌癥蛋白標志物CEA,CA19-9,CA72-4等更優(yōu)越的診斷效果(靈敏度0.925:0.428)。10-DM模型的準確性和重現(xiàn)性在覆蓋521人的多中心隊列中得到證實,表明該模型具有較高的穩(wěn)健性和臨床應用潛力。此外,28-PM預后模型比利用臨床參數(shù)的傳統(tǒng)模型的預測效果更好(C-index值0.816:0.591),并能有效地將患者分為高低兩個風險組。在中位數(shù)為40個月的隨訪期間,28-PM模型區(qū)分的高風險患者的預后與低風險患者相比更差,證明了模型的預測能力。被分層為高危險組的患者更有可能受益于強化監(jiān)測、及時干預和新型治療藥物的試驗。
該研究描述了胃癌患者血漿的整體代謝重編程,并結合機器學習算法構建了兩個模型,分別識別胃癌患者并預測其預后,有助于進一步理解胃癌的分子病理學特征,促進了胃癌早期檢測的發(fā)展,并為實現(xiàn)胃癌的精準治療提供理論基礎。
迄今為止報道的胃癌組學研究主要集中在探究以DNA、RNA和蛋白質作為胃癌生物標志物的潛力,而該工作強調了胃癌中循環(huán)代謝物的預測價值。通過使用高靈敏代謝組學技術分析覆蓋共計702例胃癌和非胃癌對照的多中心樣本已經獨立測試集的設定,該研究成功應對了生物標志物探究工作普遍面臨的結果再現(xiàn)性低,無法進行臨床推廣應用的挑戰(zhàn)。未來可以通過建立靶向兩個模型中代謝物的特定子集的靶向定量代謝組學檢測方法以提高效率并降低成本,并在來自更多中心的更大規(guī)模臨床樣本中進行驗證和優(yōu)化。此外,基于這兩種預測模型有望促進胃癌無創(chuàng)早期檢測,并根據(jù)患者的風險分層為臨床決策提供信息,從而實現(xiàn)輔助胃癌精準診療策略的臨床轉化。
相關研究以“代謝組學結合人工智能在準確診斷胃癌及預測患者預后中的臨床應用潛能”(Metabolomic machine learning predictor for diagnosis and prognosis of gastric cancer)為題,發(fā)表于《自然·通訊》(Nature Communications)。
清華大學藥學院2021級博士生陳洋子、趙宜滋,博士后王博弘、王銘鑠,中國醫(yī)學科學院腫瘤醫(yī)院博士邵欣欣、馬福海為論文共同第一作者。胡澤平、哈爾濱醫(yī)科大學附屬腫瘤醫(yī)院主任韓鵬、中國醫(yī)學科學院腫瘤醫(yī)院主任田艷濤為論文共同通訊作者。藥學院2020級博士生姚珂、博士后聶萌(現(xiàn)任首都醫(yī)科大學副教授)為該研究作出了重要貢獻。上海期智研究院研究員楊天舒和李蓬院士為該研究提供了大力支持和幫助。研究得到國家自然科學基金委、清華-北大生命聯(lián)合中心等的支持。
論文鏈接:
http://doi.org/10.1038/S41467-024-46043-Y
供稿:藥學院
題圖設計:李娜
編輯:李華山
審核:郭玲
