清華新聞網(wǎng)5月28日電 常見慢性疾病是人類健康的主要威脅,這些疾病涉及人體所有器官系統(tǒng),發(fā)病率高、不可避免且無法治愈,導(dǎo)致沉重的疾病、經(jīng)濟(jì)和社會(huì)負(fù)擔(dān)。哮喘是呼吸系統(tǒng)最常見的疾病,全球有超過3億哮喘患者,每年約有25萬人死于重癥哮喘。與其他常見慢性疾病一樣,哮喘是一種不可治愈的終身疾病,患者需要終生服藥。
2型炎癥因子(如IL-4、IL-5和IL-13等)在哮喘中發(fā)揮關(guān)鍵致病作用。目前,使用蛋白質(zhì)藥物(如抗體)阻斷2型炎癥因子對哮喘具有一定療效,并降低了糖皮質(zhì)激素的使用量。然而,蛋白質(zhì)藥物和傳統(tǒng)的小分子藥物一樣,需要長期甚至終生輸注,長期使用后會(huì)出現(xiàn)副作用,患者也會(huì)產(chǎn)生針對這些蛋白質(zhì)的抗體,導(dǎo)致療效下降。因此,蛋白質(zhì)藥物對哮喘的療效有限,也無法根治哮喘。
與傳統(tǒng)的小分子和蛋白質(zhì)藥物需要終生給藥不同,嵌合抗原受體T(CAR-T)細(xì)胞作為活體藥物,其在體內(nèi)的持久性賦予了其治愈慢性疾病的潛力。目前,CAR-T細(xì)胞對一部分B細(xì)胞白血病患者達(dá)到了臨床治愈,但CAR-T細(xì)胞是否可以治愈非腫瘤慢性疾病尚無先例。
5月27日,清華大學(xué)基礎(chǔ)醫(yī)學(xué)院彭敏副教授團(tuán)隊(duì)在《自然·免疫學(xué)》(Nature Immunology)雜志發(fā)表了題為“單次輸入長壽命多功能T細(xì)胞在小鼠模型中長期緩解哮喘”(A single infusion of engineered long-lived and multifunctional T cells confers durable remission of asthma in mice)的研究論文。該研究報(bào)道了一種基于長壽命CAR-T細(xì)胞的哮喘治愈性療法,僅需單次輸入經(jīng)過基因編輯和改造的長效多功能CAR-T細(xì)胞,即可在動(dòng)物模型中實(shí)現(xiàn)對哮喘的長期療效,達(dá)到治愈效果。該研究首次實(shí)現(xiàn)了CAR-T細(xì)胞對哮喘這一常見疾病在動(dòng)物模型中的治愈,開啟了細(xì)胞療法治愈常見非腫瘤疾病的新篇章。
目前,CAR-T細(xì)胞治療非腫瘤慢性疾病面臨三大障礙。首先,大部分常見慢性疾病的病因復(fù)雜且不可移除(如環(huán)境、衰老等),病情反復(fù),持續(xù)終生。這要求用于治療的CAR-T細(xì)胞具備終生持久性,即輸入一次,終生存在,終生有效。其次,目前CAR-T細(xì)胞治療需要對患者進(jìn)行基于化療的預(yù)處理(即“清淋”),但這對于非腫瘤患者而言是不可接受的,因?yàn)榛煏?huì)帶來嚴(yán)重副作用。第三,與腫瘤不同,慢性疾病累及的細(xì)胞(如心、肝、肺、腎、腦等)不能簡單地通過CAR-T細(xì)胞清除,因?yàn)檫@些組織器官具有不可或缺的生理功能。因此,選擇合適的CAR-T靶點(diǎn)尤為重要。
為了解決CAR-T細(xì)胞療效持久性和化療預(yù)處理問題,彭敏團(tuán)隊(duì)首先以臨床上最常用的CD19 CAR-T細(xì)胞為模型,通過全基因CRISPR篩選發(fā)現(xiàn)了基因組中一個(gè)特殊的基因組合,即BCOR和ZC3H12A。敲除這兩個(gè)基因使得CAR-T細(xì)胞進(jìn)入一種全新的狀態(tài),被命名為“類永生化功能性”T細(xì)胞(Immortal-like and Functional T cells,簡稱TIF)。CARTIF細(xì)胞具備類似于誘導(dǎo)多功能干細(xì)胞(iPSCs)的無限自我更新能力,可在體內(nèi)終生存在。然而,與iPSCs不同的是,CARTIF細(xì)胞不會(huì)因?yàn)楂@得干性而失去譜系特征和功能,而是完整保留了成熟T細(xì)胞的特性和生理功能。因此,TIF代表了一種新的哺乳動(dòng)物細(xì)胞存在形式,即干性(stemness)和功能性(functionality)共存于同一細(xì)胞。CARTIF細(xì)胞在腫瘤模型中表現(xiàn)出了優(yōu)異的療效。彭敏團(tuán)隊(duì)的這一發(fā)現(xiàn)于3月26日發(fā)表于《實(shí)驗(yàn)醫(yī)學(xué)雜志》(J Exp Med),題為“通過特定的因素誘導(dǎo)類永生化功能性CAR-T細(xì)胞”(Induction of immortal-like and functional CAR T cells by defined factors),并得到了CAR-T細(xì)胞領(lǐng)域?qū)<业母叨仍u價(jià)。更為重要的是,CARTIF細(xì)胞在體內(nèi)的擴(kuò)增和維持不需要對宿主進(jìn)行任何預(yù)處理,非常適合用于治療非腫瘤疾病。
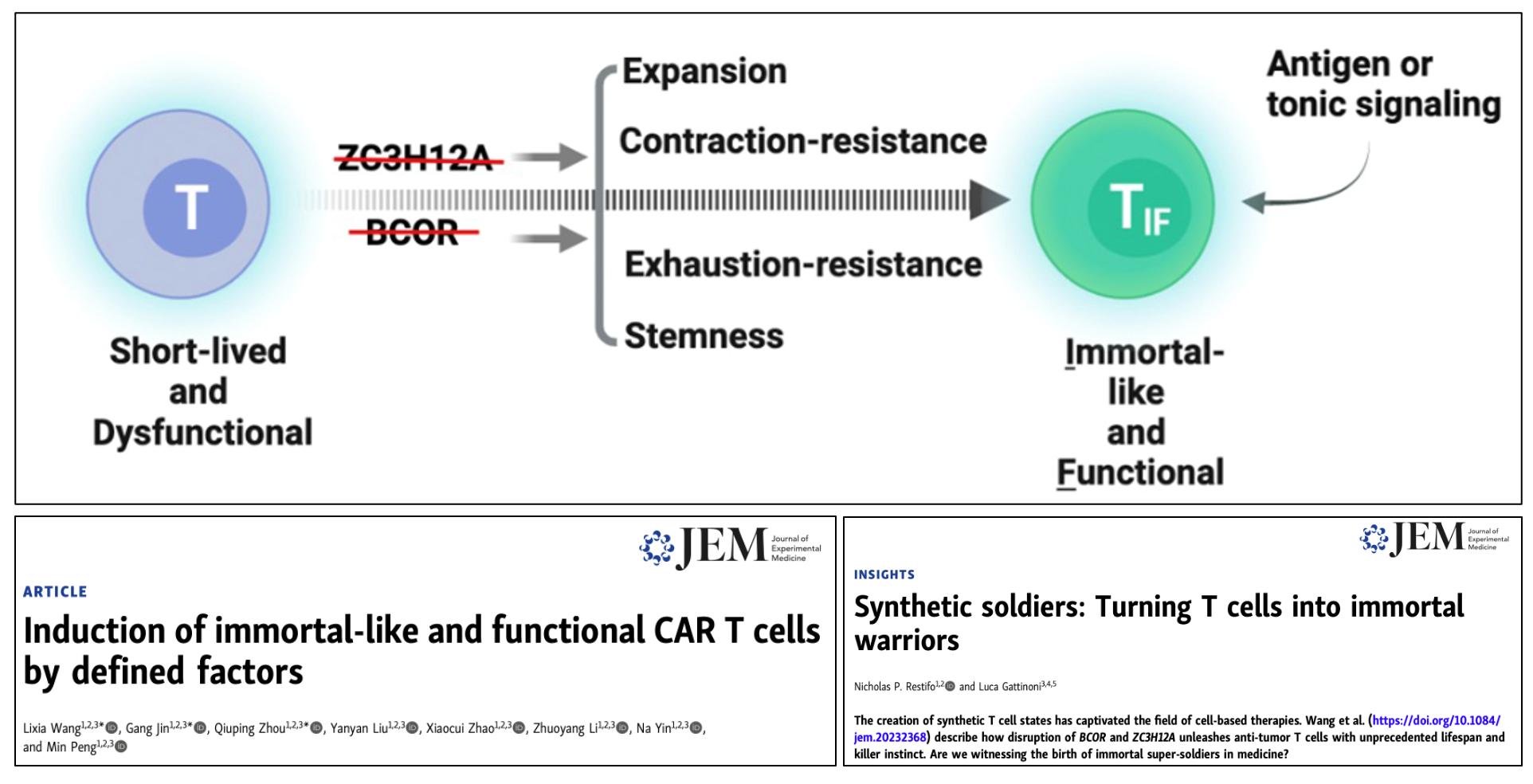
圖1.類永生化功能性T細(xì)胞(TIF)的誘導(dǎo)機(jī)制及專家點(diǎn)評
解決了CAR-T細(xì)胞的持久性和化療預(yù)處理問題后,彭敏團(tuán)隊(duì)將CARTIF這一全新概念和技術(shù)平臺應(yīng)用于呼吸系統(tǒng)最常見的疾病——哮喘。IL-5介導(dǎo)的嗜酸性粒細(xì)胞浸潤是2型哮喘的重要病理特征,臨床上使用嗜酸性粒細(xì)胞的清除抗體對2型哮喘具有一定療效。彭敏團(tuán)隊(duì)以IL-5為CAR的抗原結(jié)合域,構(gòu)建了識別并殺傷嗜酸性粒細(xì)胞(高表達(dá)IL-5受體)的IL-5 CAR-T細(xì)胞。雖然IL-5 CAR-T細(xì)胞在體外可特異性識別和殺傷嗜酸性粒細(xì)胞,但無法在體內(nèi)擴(kuò)增。彭敏團(tuán)隊(duì)通過基因編輯將上述TIF程序植入IL-5 CAR-T細(xì)胞,使得該細(xì)胞可以在無需任何預(yù)處理的條件下在免疫健全小鼠中增殖并清除嗜酸性粒細(xì)胞,且終生存在。該細(xì)胞被命名為5TIF細(xì)胞。鑒于IL-4和IL-13在2型哮喘中的關(guān)鍵致病作用,5TIF細(xì)胞被進(jìn)一步改造用于長期分泌一種可以同時(shí)抑制IL-4和IL-13的IL-4突變體,并將其命名為5TIF4細(xì)胞。在多種哮喘模型中,單次輸入5TIF4細(xì)胞即可實(shí)現(xiàn)對嗜酸性粒細(xì)胞的長期清除和對IL-4和IL-13的持續(xù)性抑制,顯著緩解肺部炎癥,消除哮喘癥狀,達(dá)到治愈效果。該研究還在NSG小鼠中驗(yàn)證了人5TIF4細(xì)胞的可行性,為將來的臨床試驗(yàn)打下基礎(chǔ)。
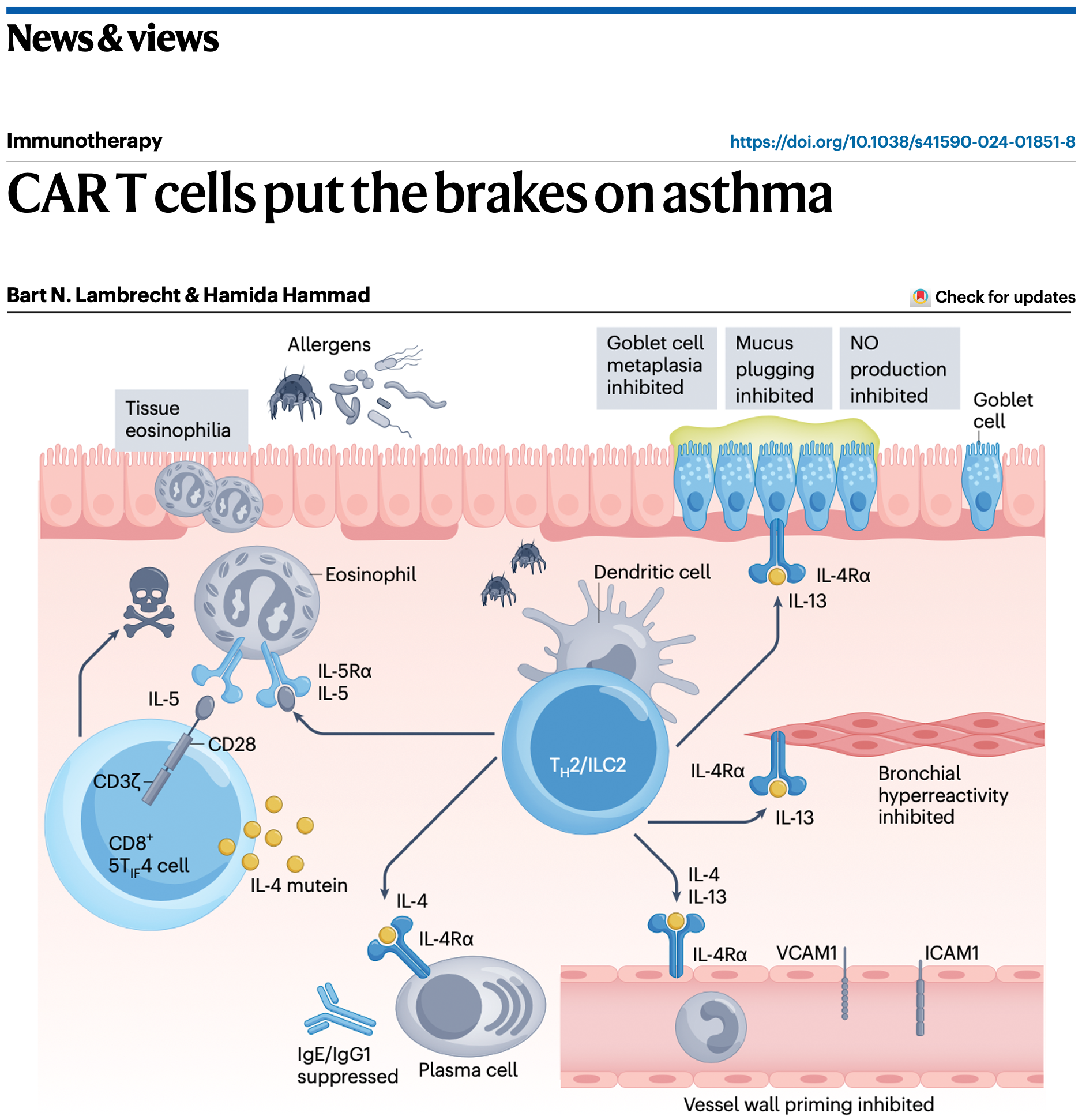
圖2.哮喘領(lǐng)域著名專家對5TIF4細(xì)胞的點(diǎn)評
《自然·免疫學(xué)》(Nature Immunology)期刊邀請了哮喘領(lǐng)域的國際著名學(xué)者哈米達(dá)·哈馬德(Hamida Hammad)教授等就該研究發(fā)表了題為“CAR-T細(xì)胞抑制了哮喘”(CAR T cells put the brakes on asthma)的評述文章。哈米達(dá)·哈馬德教授認(rèn)為,5TIF4細(xì)胞很好地解決了目前CAR-T細(xì)胞治療非腫瘤疾病存在的各種問題,是一種開創(chuàng)性的療法,具備治愈哮喘的可能性。同時(shí),哈米達(dá)·哈馬德也指出了5TIF4細(xì)胞可能存在的副作用、如何選擇患者以及進(jìn)一步降低CAR-T細(xì)胞制造成本對于推廣該療法的重要性。
綜上所述,該研究首次報(bào)道了針對哮喘的單次輸入治愈性細(xì)胞療法,為呼吸系統(tǒng)這一常見疾病的根治提供了新思路和臨床前產(chǎn)品。未來,這一研究有望為數(shù)以億計(jì)的哮喘患者(尤其是重癥哮喘患者)帶來“一勞永逸”的療法,改寫慢性疾病不可治愈的歷史。
彭敏為該論文通訊作者,彭敏團(tuán)隊(duì)成員金剛(博士后,彭敏實(shí)驗(yàn)室2017級博士生)和劉巖巖(2020級博士生)為該論文共同第一作者。彭敏實(shí)驗(yàn)室致力于T細(xì)胞基礎(chǔ)和應(yīng)用研究,長期目標(biāo)是通過細(xì)胞療法治愈人類常見疾病。
論文鏈接:
https://www.nature.com/articles/s41590-024-01834-9
https://doi.org/10.1084/jem.20232368
https://www.nature.com/articles/s41590-024-01851-8
供稿:基礎(chǔ)醫(yī)學(xué)院
編輯:李華山
審核:郭玲
