清華新聞網(wǎng)5月31日電 CRISPR系統(tǒng)是一種存在于原核生物中的適應(yīng)性免疫系統(tǒng),用于抵御外來DNA的入侵。在長期的免疫防御斗爭中,CRISPR系統(tǒng)已經(jīng)演化成多種類型,其中,Cas9通過引導(dǎo)RNA(gRNA)切割外源DNA的特性被廣泛研究和應(yīng)用到基因編輯領(lǐng)域。Cas9系統(tǒng)具有多種亞型,如II-A、II-B和II-C,其中II-C型的Cas9的多樣性最高。然而CRISPR-Cas9系統(tǒng)是否存在額外的機(jī)制以對抗病毒的免疫逃逸競爭尚且未知,通過挖掘并解析這些未知的機(jī)制,有助于進(jìn)一步拓展我們對于CRISPR系統(tǒng)進(jìn)化過程的了解并且進(jìn)一步提升其基因編輯效率。
5月29日,清華大學(xué)生命學(xué)院劉俊杰(Jun-Jie Gogo Liu)課題組聯(lián)合北京大學(xué)生命學(xué)院白洋課題組和清華大學(xué)生命學(xué)院陳春來課題組在《自然》(Nature)雜志在線發(fā)表了題為“CRISPR免疫增效子PcrIIC1增強(qiáng)細(xì)菌Cas9系統(tǒng)免疫能力”(Pro-CRISPR PcrIIC1-associated Cas9 system for enhanced bacterial immunity)的研究論文。
通過生物信息學(xué)分析,研究團(tuán)隊(duì)觀察到一類新型關(guān)聯(lián)基因(Novel-associated genes, NAGs),顯著富集存在于較大蛋白體積的II-C型Cas9的基因簇中,并推測這些NAGs可能參與到Cas9介導(dǎo)的細(xì)菌免疫過程中。為了進(jìn)一步探索Cas9和NAGs的關(guān)系,研究人員開發(fā)了一套結(jié)構(gòu)生長軌跡分析方法(structural growth trajectory analysis, SGT analysis),通過預(yù)測1381個(gè)II-C型Cas9的蛋白結(jié)構(gòu),實(shí)現(xiàn)了對Cas9蛋白結(jié)構(gòu)演變的量化和軌跡分析。通過分析,發(fā)現(xiàn)了較大蛋白體積的II-C型Cas9存在自身新功能結(jié)構(gòu)域生長進(jìn)化的趨勢,呈現(xiàn)出三條不同的蛋白體積逐漸變大的進(jìn)化軌跡。研究人員還發(fā)現(xiàn)與NAGs的協(xié)同作用富集在三條生長軌跡的終點(diǎn),這可能說明在漫長的進(jìn)化過程中,Cas9系統(tǒng)新功能結(jié)構(gòu)域的插入和NAGs的出現(xiàn)具有一定的相關(guān)性。
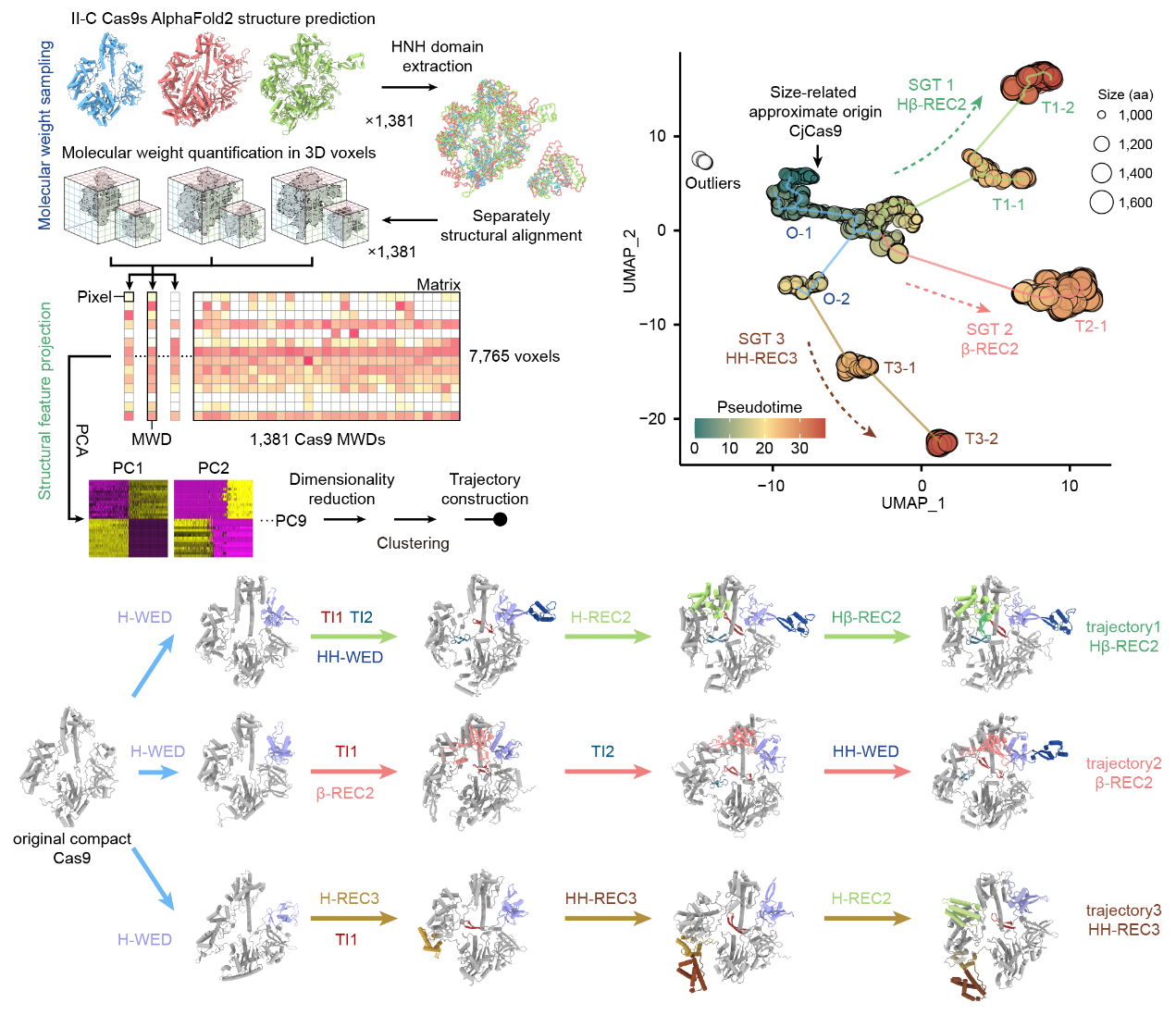
圖1.結(jié)構(gòu)生長軌跡分析方法(左)和II-C型Cas9的生長軌跡圖(右)
研究團(tuán)隊(duì)通過生化實(shí)驗(yàn)和冷凍電鏡解析復(fù)合體結(jié)構(gòu)表明,來自金黃色細(xì)菌屬(Chryseobacteriumsp.)的CbCas9生長出了一個(gè)全新的增強(qiáng)Cas9活性的β-REC2結(jié)構(gòu)域,以及一個(gè)全新的能夠與其關(guān)聯(lián)基因PcrIIC1互作的CTH結(jié)構(gòu)域。通過蛋白間相互作用,2個(gè)CbCas9蛋白和2個(gè)PcrIIC1蛋白能夠形成異源四聚體復(fù)合物。
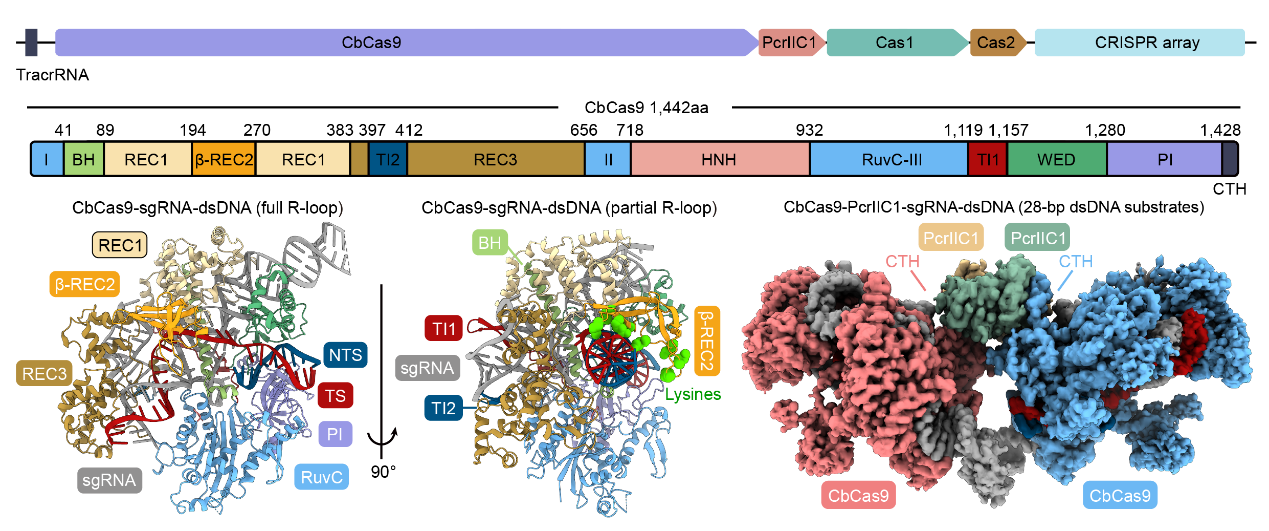
圖2.CbCas9基因簇構(gòu)成(上)、CbCas9效應(yīng)蛋白結(jié)構(gòu)(左下)和CbCas9-PcrIIC1復(fù)合體結(jié)構(gòu)(右下)
研究團(tuán)隊(duì)發(fā)現(xiàn),PcrIIC1蛋白能夠作為一種CRISPR免疫增效子(Pro-CRISPR),通過與CbCas9形成異源四聚體復(fù)合體增強(qiáng)其活性。CbCas9-PcrIIC1復(fù)合物表現(xiàn)出增強(qiáng)的DNA結(jié)合和切割活性,更廣泛的前間隔序列鄰近基序(PAM)兼容性,更強(qiáng)的DNA雙鏈解旋能力以及對靶向序列互補(bǔ)錯配(mismatch)的容忍能力。

圖3.PcrIIC1增強(qiáng)CbCas9的DNA結(jié)合(a)、切割(b)、PAM兼容性(c)、DNA解旋(d)和錯配容忍(e)能力
為了進(jìn)一步探究PcrIIC1增強(qiáng)Cas9活性的具體機(jī)制,研究人員進(jìn)一步通過結(jié)構(gòu)解析發(fā)現(xiàn),CbCas9-PcrIIC1復(fù)合物的能力增強(qiáng)來源于復(fù)合物中的兩個(gè)CbCas9能夠結(jié)合同一條長鏈DNA,通過更強(qiáng)的電荷相互作用,使得該復(fù)合物的DNA結(jié)合能力增強(qiáng)。并且,復(fù)合體中的兩個(gè)CbCas9通過協(xié)同作用,使得長鏈DNA發(fā)生扭曲和變構(gòu),更容易被解旋,從而促進(jìn)了CbCas9-PcrIIC1復(fù)合物的DNA干擾(interference)能力。同時(shí),研究團(tuán)隊(duì)還發(fā)現(xiàn),兩個(gè)CbCas9能夠?qū)ΨQ地分別靶向長鏈DNA的兩條單鏈上的靶標(biāo)序列,從而提高其在基因組上搜尋靶標(biāo)的效率。
最終,為了檢驗(yàn)CRISPR免疫增效子PcrIIC1對CbCas9抗噬菌體免疫能力的影響,研究人員在大腸桿菌中進(jìn)行了抗噬菌體實(shí)驗(yàn)。實(shí)驗(yàn)結(jié)果表明PcrIIC1顯著提升CbCas9系統(tǒng)對噬菌體的抵抗,且如果破壞CbCas9與PcrIIC1的相互作用,會導(dǎo)致增強(qiáng)的免疫力喪失。以上結(jié)果說明CbCas9-PcrIIC1復(fù)合體的形成對整個(gè)CRISPR-Cas系統(tǒng)的免疫增強(qiáng)至關(guān)重要。
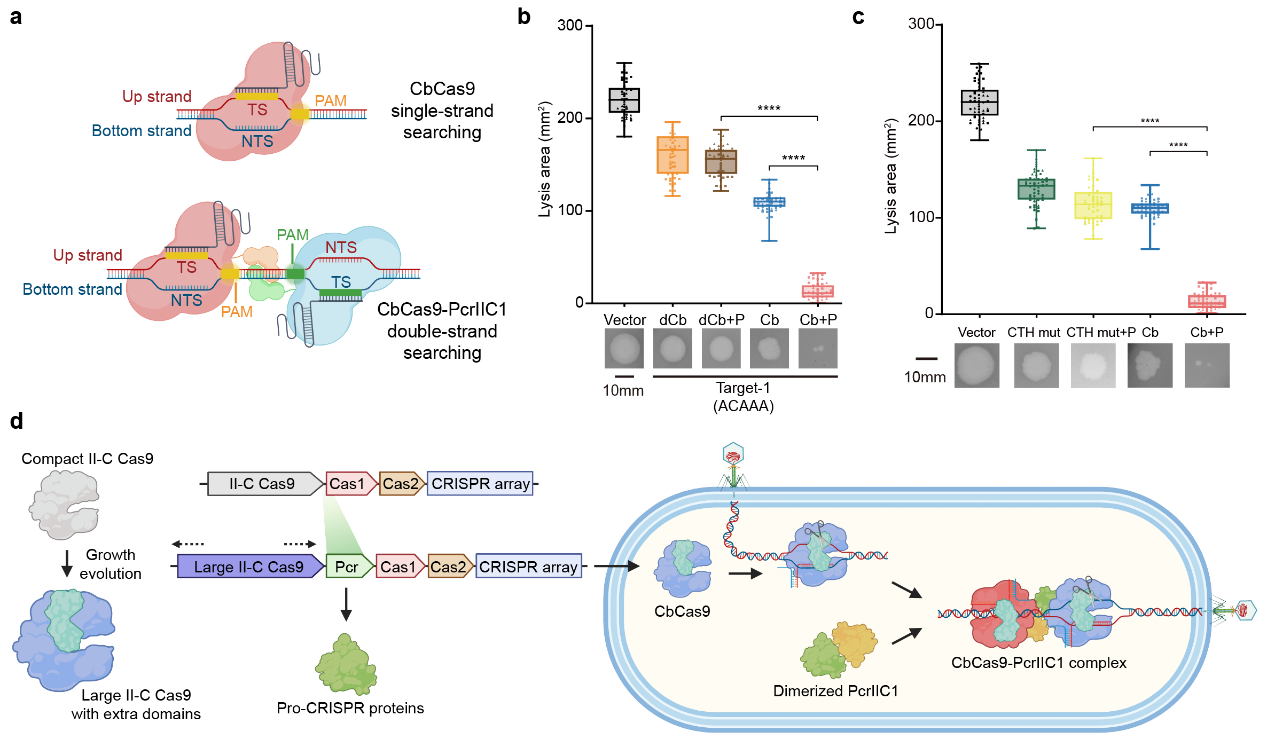
圖4.PcrIIC1顯著增強(qiáng)了CbCas9系統(tǒng)的細(xì)菌免疫活性
研究開發(fā)了一套基于結(jié)構(gòu)的SGT進(jìn)化軌跡分析,鑒定出II-C亞型Cas9的進(jìn)化趨勢,首次發(fā)現(xiàn)了一類新型的CRISPR免疫增效子可以通過二聚化Cas9效應(yīng)器提升Cas9活性,這些結(jié)果不僅有助于我們進(jìn)一步理解CRISPR系統(tǒng)的進(jìn)化歷程,還為未來基于CRISPR免疫增效子的高效基因編輯工具的開發(fā)奠定了基礎(chǔ)。
清華大學(xué)生命學(xué)院劉俊杰副教授、北京大學(xué)生命學(xué)院白洋研究員和清華大學(xué)生命學(xué)院陳春來副教授為論文通訊作者;清華大學(xué)生命學(xué)院博士后張壽悅、2020級博士生孫奧、中國科學(xué)院遺傳與發(fā)育生物學(xué)研究所2017級直博生錢景美和清華大學(xué)生命學(xué)院2023級博士生林鑠為論文共同第一作者。中國科學(xué)院遺傳與發(fā)育生物學(xué)研究所高彩霞課題組、北京生命科學(xué)研究所董夢秋課題組對研究給予了大力支持。研究得到國家重點(diǎn)研發(fā)計(jì)劃、自然科學(xué)基金委、農(nóng)業(yè)部、科學(xué)探索獎和清華大學(xué)與北京大學(xué)的經(jīng)費(fèi)、資源支持。
論文鏈接:
https://www.nature.com/articles/s41586-024-07486-x
供稿:生命學(xué)院
編輯:李華山
審核:郭玲
