清華新聞網(wǎng)10月10日電 近日,清華大學(xué)藥學(xué)院儲(chǔ)凌課題組研究開發(fā)了一種由4,4'-二聯(lián)吡啶介導(dǎo)的芳硝基還原方法,在生物兼容的環(huán)境下實(shí)現(xiàn)含硝基前藥的激活,該方法為藥物遞送提供了新的工具。
在癌癥治療中,前藥的開發(fā)是降低毒副作用和提高藥物遞送效率的手段之一。生物正交反應(yīng)和點(diǎn)擊化學(xué)的發(fā)展為前藥活化提供了新的思路,其中SQP33是一種被反式環(huán)烯烴(TCO)修飾的阿霉素前藥,毒性被減弱的同時(shí)進(jìn)行全身注射,通過局部注射四嗪(Tz)修飾的生物聚合物來(lái)進(jìn)行局部激活。在這一過程中精準(zhǔn)的給藥途徑以及高效選擇性的點(diǎn)擊化學(xué)共同實(shí)現(xiàn)特異性靶向,因此快速高效的生物正交反應(yīng)的發(fā)展是推動(dòng)這一領(lǐng)域發(fā)展的關(guān)鍵。
在芳硝基還原的前藥開發(fā)中,利用實(shí)體瘤缺氧的特性開發(fā)的缺氧激活前藥(HAP)依靠腫瘤缺氧環(huán)境中過表達(dá)的內(nèi)源性還原酶還原釋放細(xì)胞毒素,然而這一方法受限于實(shí)體瘤的復(fù)雜異質(zhì)性,以及臨床上缺乏可靠的缺氧生物標(biāo)志物。硝基還原酶的異源表達(dá)是激活芳香硝基前藥的另一種策略,然而該方法的推廣同樣受限于酶催化效率與基因轉(zhuǎn)染效率。
為了進(jìn)一步推進(jìn)芳香族硝基前藥在癌癥治療中的應(yīng)用,需要新的策略來(lái)規(guī)避腫瘤細(xì)胞固有的生物學(xué)特性,提高其激活效率。儲(chǔ)凌課題組提出了4,4'-二聯(lián)吡啶介導(dǎo)的芳硝基還原反應(yīng)用于前藥激活的策略(圖1)。這是一個(gè)由有機(jī)催化劑介導(dǎo)的生物正交反應(yīng)方法,反應(yīng)在低濃度微摩爾級(jí)和生物相容條件下進(jìn)行,同時(shí)發(fā)現(xiàn)水在低底物濃度下起著關(guān)鍵作用。這種前藥激活反應(yīng)在哺乳動(dòng)物細(xì)胞、細(xì)菌和動(dòng)物模型中是兼容的。此外,該研究展示了一個(gè)4,4'-聯(lián)吡啶介導(dǎo)的還原環(huán)化級(jí)聯(lián)反應(yīng),用于在活細(xì)胞中合成吲哚衍生物。
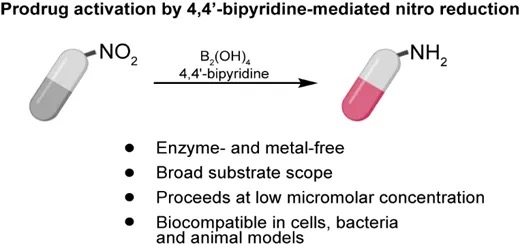
圖1.4,4'-二聯(lián)吡啶介導(dǎo)的芳香硝基還原在細(xì)胞、細(xì)菌和動(dòng)物模型中的前藥激活
為了測(cè)試該硝基還原反應(yīng)是否在活細(xì)胞中兼容,研究人員首先用熒光探針2d以及前體1d孵育細(xì)胞(圖2A),1d的熒光通過PeT效應(yīng)被硝基猝滅,1d被還原后則會(huì)恢復(fù)熒光。通過共聚焦顯微鏡觀察到,添加B2(OH)4和4,4'-二聯(lián)吡啶增加了細(xì)胞的熒光強(qiáng)度(圖2B),表明該反應(yīng)可以在生物相容條件下進(jìn)行。通過熒光強(qiáng)度定量分析發(fā)現(xiàn),反應(yīng)收率在20%-40%之間(圖2C)。
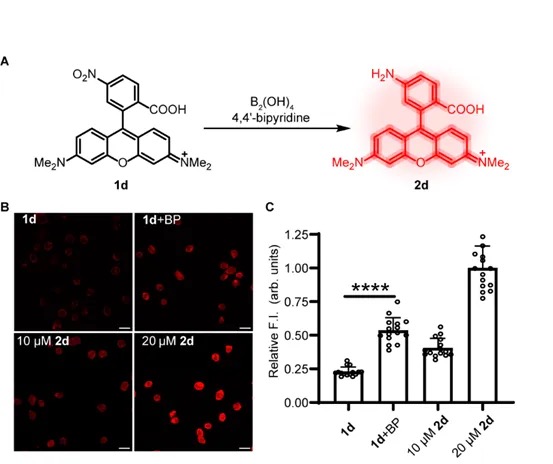
圖2. 活細(xì)胞中1d硝基的還原
甲氧芐啶(TMP)和磺胺的協(xié)同給藥用于治療細(xì)菌感染。研究人員嘗試將硝基還原的方法用于抗菌前藥的激活。研究人員首先優(yōu)化了TMP和磺胺二甲嘧啶(SMZ)的濃度比例,以達(dá)到最大的細(xì)菌生長(zhǎng)抑制效果。結(jié)果顯示,0.44μM TMP與44μM SMZ組合的協(xié)同效應(yīng)最高(圖3C)。在接下來(lái)的測(cè)試中,0.44μM TMP、44μM前藥1f和B2(OH)4/4,4'-二聯(lián)吡啶的組合處理大腸桿菌的抑菌效果與0.44μM TMP、44μM 2f效果相當(dāng)(圖3D),證明了4,4'-二聯(lián)吡啶介導(dǎo)的氮還原為抗微生物治療提供了一種互補(bǔ)的前藥策略。
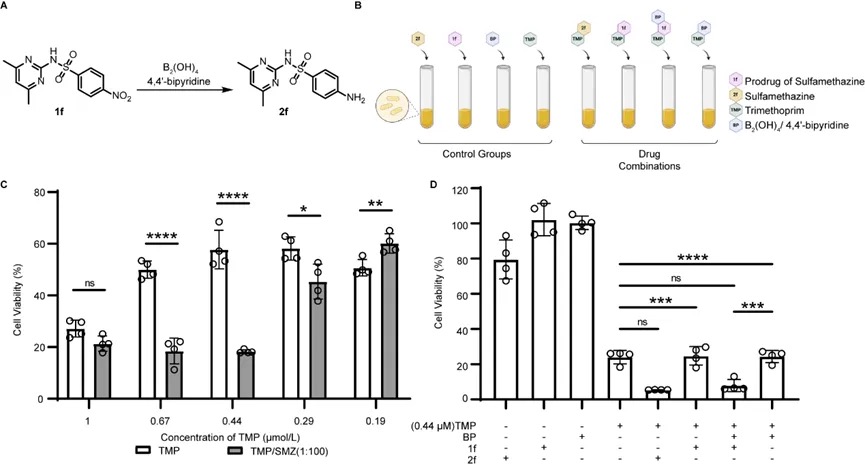
圖3.前藥1f硝基還原的抑菌作用
吲哚是一種多功能藥效團(tuán),通過不同的作用機(jī)制發(fā)揮廣泛的藥理活性。研究人員設(shè)想鄰硝基乙醛在硝基還原后可能會(huì)環(huán)化形成吲哚環(huán)(圖4A)。基于此設(shè)想合成了鄰硝基苯乙醛衍生物7,前藥7發(fā)生級(jí)聯(lián)化反應(yīng)轉(zhuǎn)化為吲哚衍生物8(圖4B),即一種抗有絲分裂藥物。當(dāng)用前藥7,B2(OH)4/4,4'-二聯(lián)吡啶共同孵育細(xì)胞后,表現(xiàn)出顯著的細(xì)胞殺傷效果(圖4C),表明在催化劑的存在下,7在細(xì)胞中轉(zhuǎn)化為8。這些實(shí)驗(yàn)表明,硝基還原-環(huán)化級(jí)聯(lián)可以作為活細(xì)胞中吲哚合成的補(bǔ)充策略。
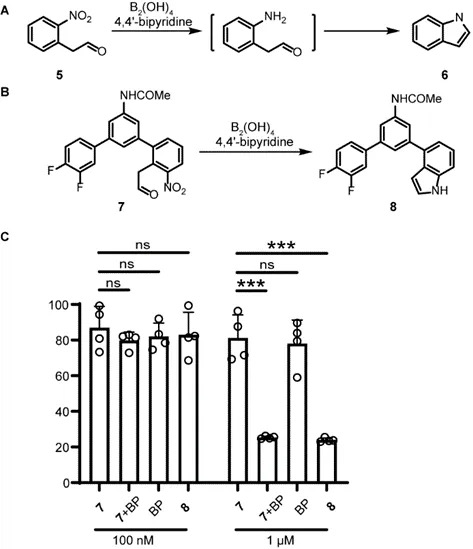
圖4.芳香硝基還原-環(huán)化級(jí)聯(lián)在活細(xì)胞中合成吲哚
工作的最后,為了證明該方法在體內(nèi)的有效性,研究人員構(gòu)建了穩(wěn)定表達(dá)Super Degron(SD)融合螢火蟲熒光素酶(FLuc)的4T1細(xì)胞系(圖5B)。SD系統(tǒng)使任何融合蛋白在IMiDs處理下都容易降解,研究人員設(shè)想Iberdomide的前藥(Pro-Iber)可以在硝基還原條件下被激活得到Iberdomide(Iber)。首先在體外測(cè)試了這個(gè)降解系統(tǒng),成功觀察到Pro-Iber+ B2(OH)4/4,4'-二聯(lián)吡啶組和Iber組的發(fā)光信號(hào)減少(圖5A),表明該策略可以成功激活Pro-Iber并降解Fluc-SD。隨后用表達(dá)FLuc- SD的4T1細(xì)胞構(gòu)建動(dòng)物模型,并成功觀察到藥物治療組的生物發(fā)光信號(hào)下降(圖5C,D)。結(jié)果表明通過硝基還原的前藥激活策略在體內(nèi)具有生物相容性,并有望實(shí)現(xiàn)靶向給藥。
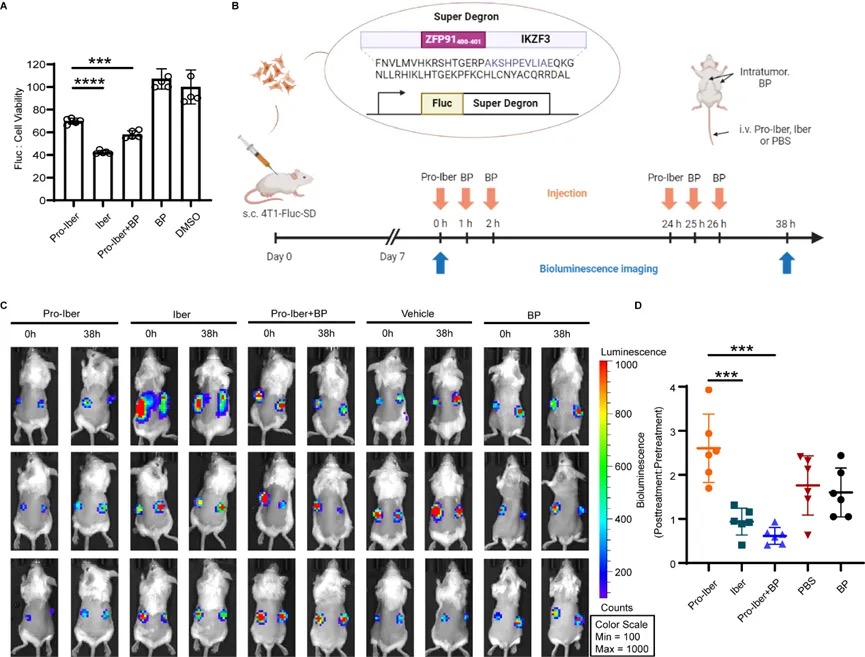
圖5.Pro-Iberdomide激活在體內(nèi)的蛋白降解
總之,該課題組報(bào)道了一個(gè)生物兼容的4,4'-二聯(lián)吡啶介導(dǎo)的芳香硝基還原反應(yīng),以控制前藥活化。該反應(yīng)顯示了良好的底物相容性,并能在低微摩爾濃度下進(jìn)行。機(jī)理研究表明水在該反應(yīng)中起著關(guān)鍵作用。通過使用熒光“turn on”底物,初步證明了該反應(yīng)與活細(xì)胞的相容性。隨后通過合成iberdomide的前藥,并在MM.1S細(xì)胞中實(shí)現(xiàn)了氮還原反應(yīng),以證明該反應(yīng)在蛋白質(zhì)降解中的應(yīng)用。此外,該前藥激活策略可以應(yīng)用于抗微生物治療。后續(xù)設(shè)計(jì)了一個(gè)用于在活細(xì)胞中合成吲哚的硝基還原-環(huán)化級(jí)聯(lián)反應(yīng),并將該級(jí)聯(lián)反應(yīng)用于合成具有生物活性的吲哚衍生物,以誘導(dǎo)癌細(xì)胞死亡。最后,通過體內(nèi)蛋白質(zhì)降解實(shí)驗(yàn),證明這種生物正交化學(xué)在動(dòng)物模型中激活前藥的能力。該方法將成為助力化學(xué)生物學(xué)和藥物遞送的寶貴工具。
相關(guān)研究成果以“一種利用4,4’-聯(lián)吡啶介導(dǎo)的硝基還原的前藥激活新策略”(Prodrug activation by 4,4’-bipyridine-mediated aromatic nitro reduction)為題,于10月5日發(fā)表于《自然·通訊》(Nature Communications)。
清華大學(xué)藥學(xué)院儲(chǔ)凌副教授為論文的通訊作者,清華大學(xué)藥學(xué)院2020級(jí)博士生王晴、博士后宋祎康(已出站)為論文的共同第一作者。清華大學(xué)藥學(xué)院博士生袁碩瑋、朱垚吉,博士后王文靜為論文提供了重要實(shí)驗(yàn)幫助。清華大學(xué)藥學(xué)院蒯銳課題組博士生何嘉提供了動(dòng)物實(shí)驗(yàn)支持。清華大學(xué)蛋白質(zhì)研究技術(shù)中心提供了液質(zhì)聯(lián)用技術(shù)支持。研究得到國(guó)家重點(diǎn)研發(fā)計(jì)劃、生物結(jié)構(gòu)前沿研究中心和清華大學(xué)“篤實(shí)計(jì)劃”、生命科學(xué)中心等的支持。
論文鏈接:
https://www.nature.com/articles/s41467-024-52604-y
供稿:藥學(xué)院
題圖設(shè)計(jì):曾儀
編輯:李華山
審核:郭玲
