清華新聞網(wǎng)3月4日電 近日,,清華大學藥學院尹航課題組研究報道了首個CRBN介導的cGAS降解劑TH35,,并探究其在潰瘍性結腸炎(UC)模型中的治療潛力,,證明了cGAS靶向降解策略在安全性和有效性上相較于抑制劑的顯著性優(yōu)勢,。
環(huán)磷酸鳥苷-腺苷合成酶(Cyclic GMP-AMP Synthase,,cGAS)是先天免疫系統(tǒng)中識別細胞質DNA的關鍵傳感器,,主要通過識別細胞內(nèi)的雙鏈DNA(dsDNA)激活免疫反應。然而,,cGAS的過度激活會引發(fā)慢性炎癥反應,,導致自身免疫性疾病的發(fā)生和發(fā)展,如在潰瘍性結腸炎(UC)中發(fā)揮重要作用,。近年來,,大量研究表明cGAS在UC中高度活化,抑制其激活能促進UC的緩解和恢復,,也有研究表明通過基因編輯技術體內(nèi)敲低cGAS可顯著抑制UC的進程,。因此,cGAS可作為治療潰瘍性結腸炎的潛在新興靶點,。
近年來,,以蛋白降解靶向嵌合體(Proteolysis-Targeting Chimeras,PROTAC)技術為代表的靶蛋白降解技術給小分子藥物開發(fā)帶來了新的希望。在此背景下,,尹航課題組提出基于PROTAC技術開發(fā)首個cGAS降解劑,,并探究其在UC小鼠模型中的抗炎活性與機制。
在cGAS PROTAC分子的設計過程中,,尹航課題組選取了對人源和鼠源cGAS均具有高親和力的cGAS抑制劑G140作為靶蛋白配體,,選擇了具有優(yōu)異理化性質和藥代動力學特征的CRBN配體(來那度胺,,沙利度胺)作為E3泛素連接酶配體。隨后以cGAS與G108(與G140結構相似的類比物)的復合物共晶結構為參考,,對G140與cGAS進行分子對接分析并發(fā)現(xiàn)G140中的甲基吡唑環(huán)和羥基乙?;鶊F與G108中的相應基團具有相似的空間布局,均暴露于溶劑區(qū),,表明這些基團可作為連接鏈附著的理想位點,。隨后,研究人員引入了不同長度和化學類型的連接鏈,,包括柔性基團(如乙二醇(PEG)鏈,、烷基鏈)和剛性基團(如哌嗪環(huán)、哌啶環(huán),、炔基烷基鏈),,并合成了系列PROTAC分子(TH1至TH42)。通過評估各分子的降解活性及其對cGAS通路的抑制效果,,系統(tǒng)探究其構效關系,,最終確定具有最佳活性的候選分子TH35(圖1)。
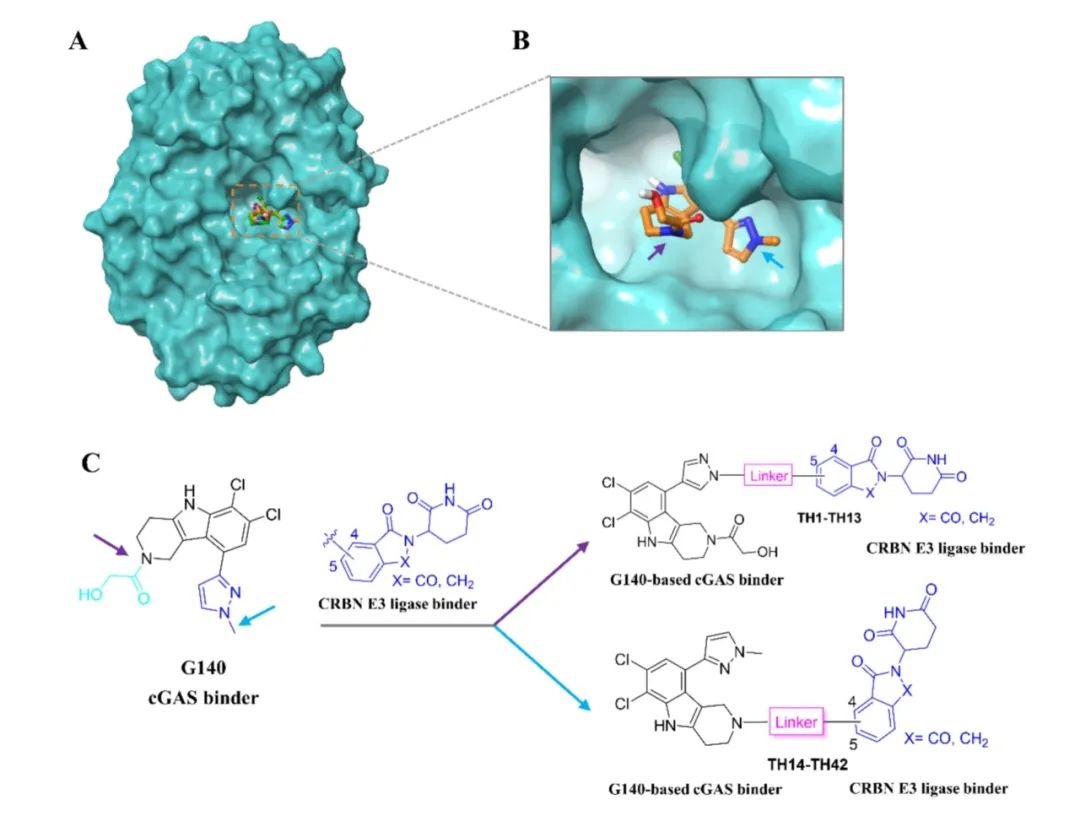
圖1.新型cGAS PROTAC降解劑的設計策略
研究發(fā)現(xiàn),,TH35在THP-1和RAW 264.7細胞中以濃度依賴性方式有效降解cGAS,,DC50值分別為0.9 ± 0.2 μM和4.6 ± 0.8 μM,最大降解率超過90%,。質譜分析顯示,,TH35顯著降低cGAS蛋白水平,且在3852個識別蛋白中,,32個蛋白的表達顯著下調,,主要為干擾素刺激基因誘導的蛋白,表明TH35通過降解cGAS抑制I型干擾素反應,?;匮a實驗結果顯示,cGAS抑制劑G140,、CRBN配體來那度胺或蛋白酶體抑制劑MG132能夠顯著逆轉TH35在THP-1細胞中的cGAS降解效應,,進一步證明TH35通過CRBN依賴的泛素-蛋白酶體途徑誘導cGAS降解(圖2)。
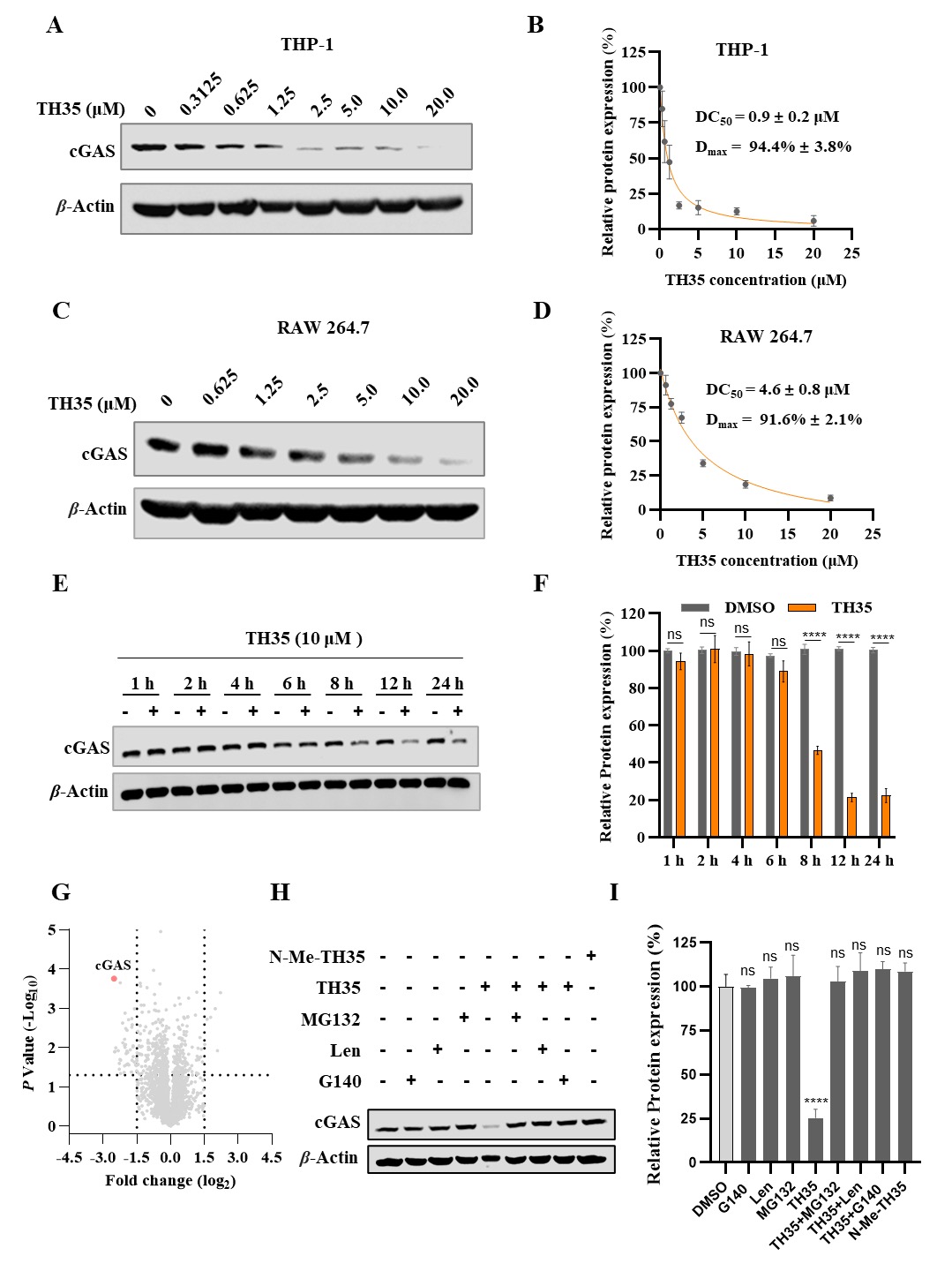
圖2.TH35的降解活性及降解機制的研究
cGAS作為細胞質中的DNA傳感器,,能夠識別細胞內(nèi)的雙鏈DNA(dsDNA),,并激活下游的STING-TBK1-IRF3信號級聯(lián)反應,在自身免疫性疾病的發(fā)病機制中扮演著關鍵角色,。定量質譜分析顯示,,TH35顯著降低了HT-DNA刺激下THP-1細胞中的cGAMP生成。熒光素酶報告基因實驗和Western blot分析進一步證明,TH35以劑量依賴方式抑制HT-DNA刺激的cGAS信號傳導及其下游關鍵蛋白(如STING,、TBK1和IRF3)的磷酸化,。此外,TH35在TREX1敲除條件下依然能顯著抑制內(nèi)源性cGAS激活,,且對由poly(I:C)和cGAMP刺激的IFNB表達沒有顯著影響,,進一步證明其較佳的特異性(圖3)。
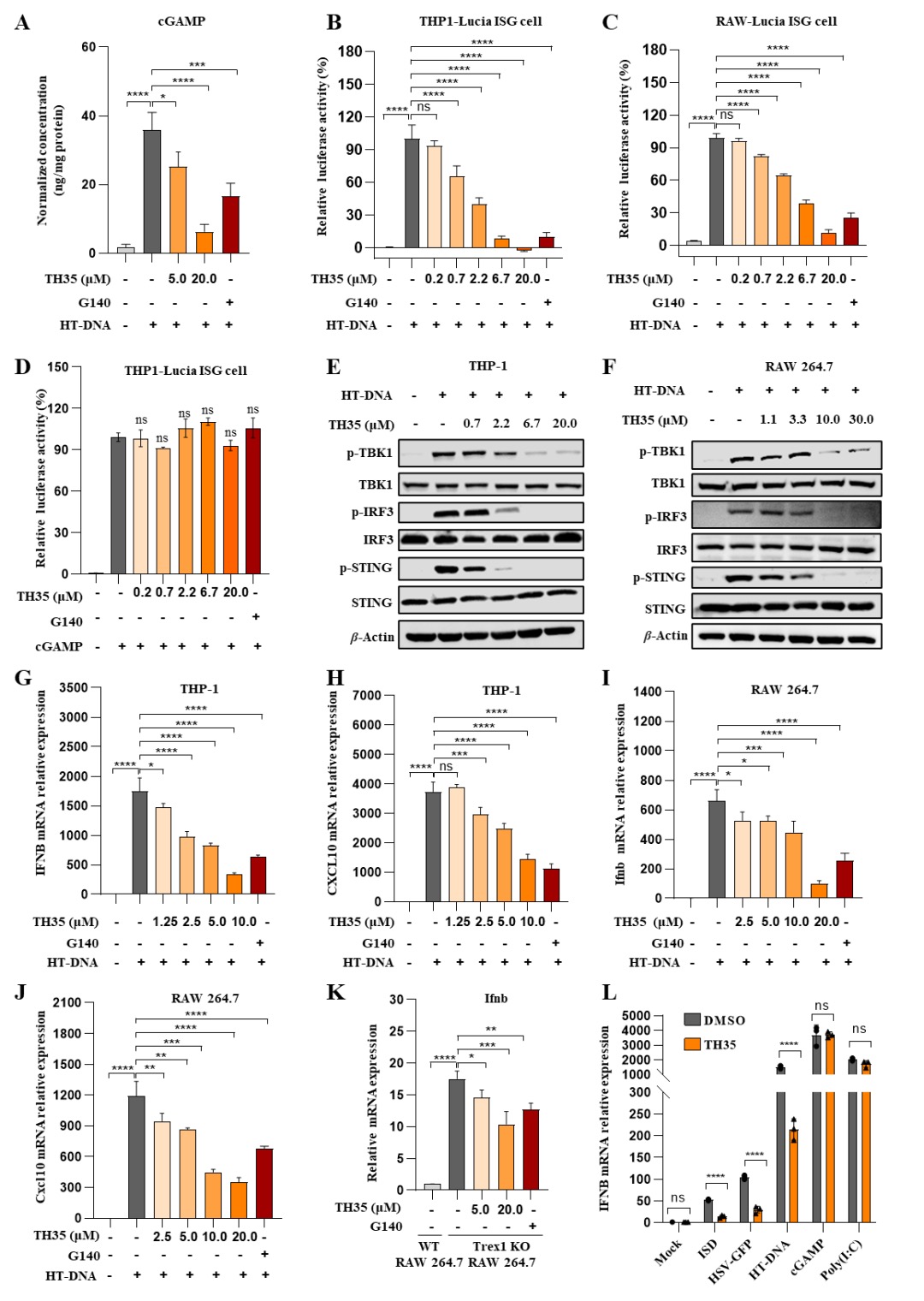
圖3.TH35選擇性抑制dsDNA誘導cGAS通路激活的研究
進一步細胞毒性評價表明,,TH35在高達60μM的濃度下對多株免疫細胞未表現(xiàn)出顯著的細胞毒性,。相比之下,,作為陽性對照的G140在超過30μM的濃度下顯著誘發(fā)細胞毒性,。這些結果表明,TH35相較于cGAS抑制劑G140展現(xiàn)出更為有利的體外安全性特征,,具有較低的脫靶毒性(圖4),。
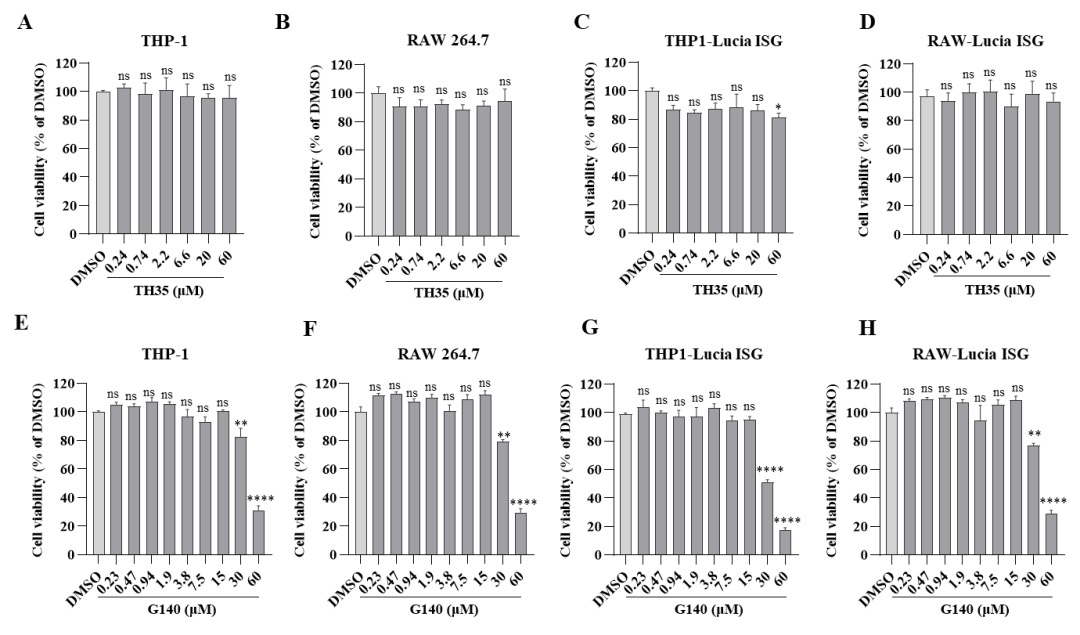
圖4.TH35與G140細胞毒性的評價
研究評估了TH35在DSS誘導的小鼠結直腸炎(UC)模型中的治療效果。實驗結果顯示,,TH35在20mg/kg和50mg/kg劑量下均顯著緩解了DSS引起的小鼠體重減輕,,且治療效果優(yōu)于傳統(tǒng)藥物5-ASA和cGAS抑制劑G140。此外,,TH35治療顯著緩解了結腸萎縮和脾腫大現(xiàn)象,,且組織學檢查顯示結腸組織病理學顯著改善,脾臟形態(tài)恢復接近正常,,病理評分低于5-ASA和G140組,。綜上,TH35在自身免疫疾病小鼠模型中相較于cGAS抑制劑G140具有更優(yōu)的抗炎活性(圖5),。
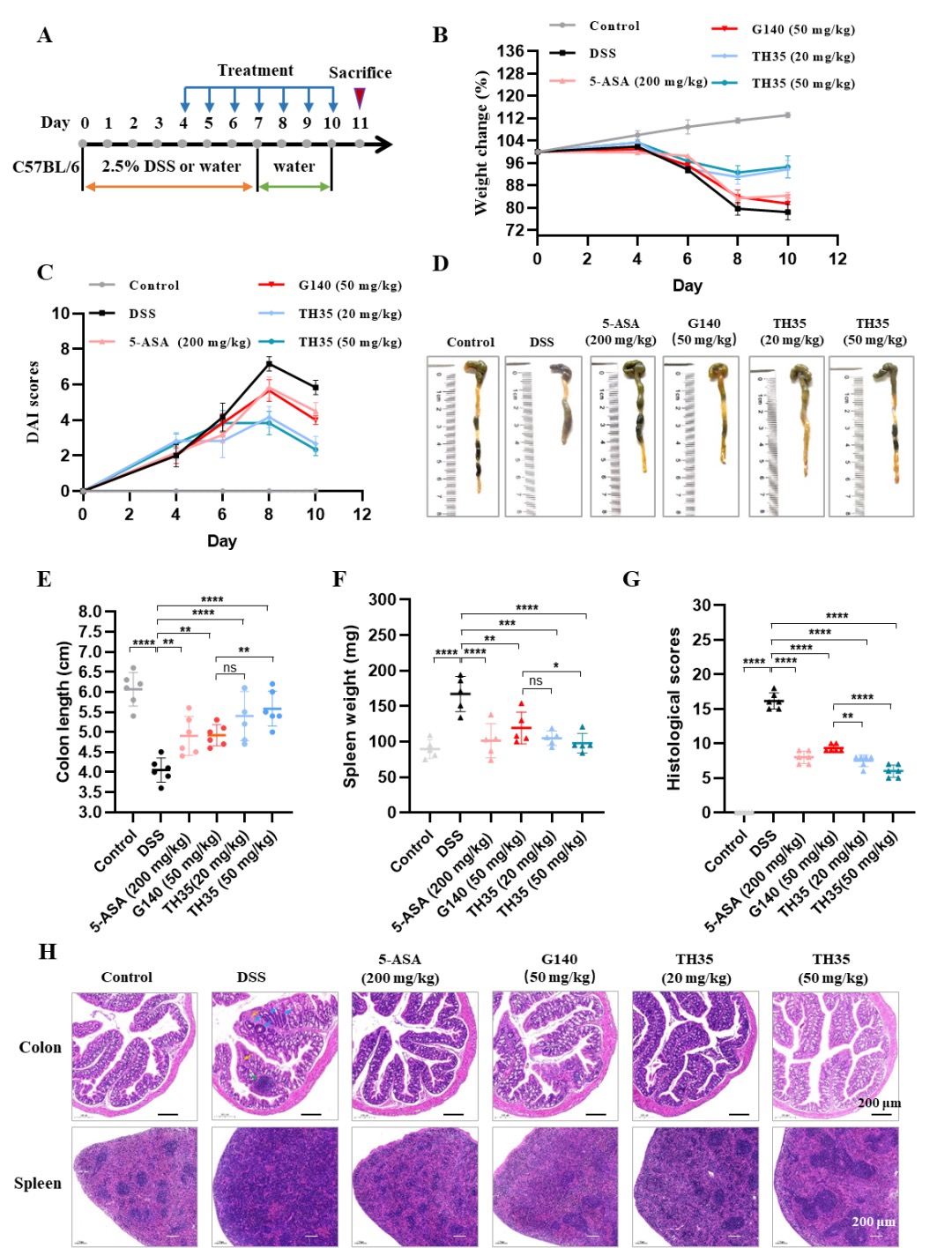
圖5.TH35體內(nèi)藥效評價
機制研究發(fā)現(xiàn),,TH35在潰瘍性結腸炎(UC)小鼠模型中通過特異性降解cGAS,顯著抑制其下游信號通路,,減少炎癥反應,。Western blot分析顯示,TH35治療劑量依賴性地降低了結腸中cGAS蛋白的表達水平,。與5-ASA和G140相比,,TH35對cGAS表達變化無顯著影響,顯示其在抗炎活性方面的不同作用機制,。RT-qPCR分析進一步表明,,TH35顯著降低了結腸中多種關鍵炎癥細胞因子的轉錄水平。此外,,TH35顯著減少了結腸組織中中性粒細胞外陷阱(NETs)的形成,,表明其在抑制NETs方面的作用優(yōu)于5-ASA和G140。
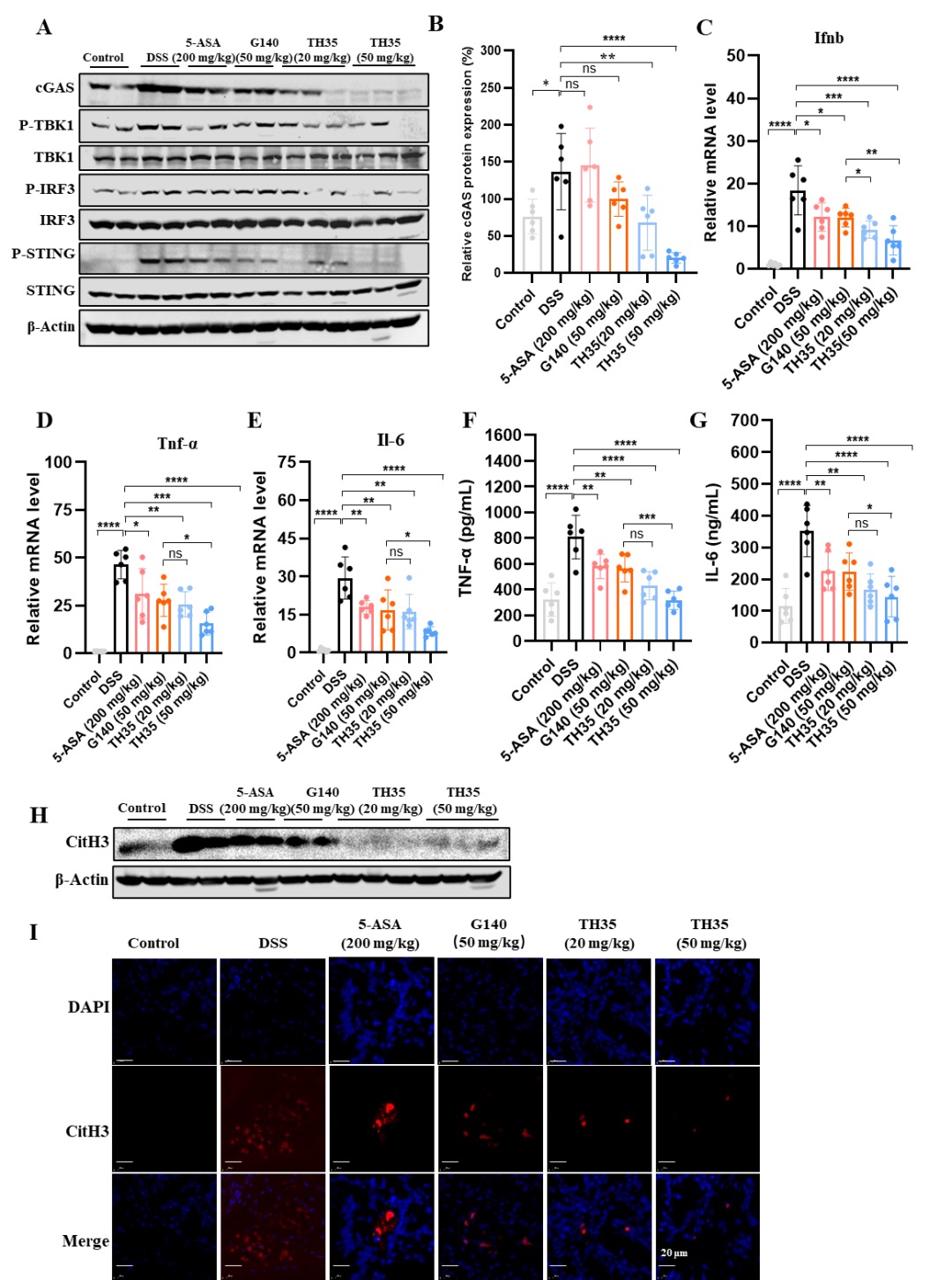
圖6.TH35體內(nèi)抗炎機制研究
該研究成功設計并報道了首個CRBN介導的cGAS PROTAC降解劑,其在體內(nèi)外抗炎活性和安全性較cGAS抑制劑具有顯著性提升,,為cGAS靶向降解治療自身免疫性疾病奠定了基礎,。
相關研究成果以“CRBN介導的新型cGAS PROTAC降解劑的發(fā)現(xiàn)及其抗?jié)冃越Y腸炎的研究”(Discovery of a Novel CRBN-Recruiting cGAS PROTAC Degrader for the Treatment of Ulcerative Colitis)為題,于2月26日發(fā)表于美國化學會的《藥物化學雜志》(Journal of Medicinal Chemistry),。
尹航為論文通訊作者,,清華大學藥學院博士后何朋和溫成銘為論文共同第一作者。清華大學藥學院博士生張新宇為本課題作出重要貢獻,。研究得到國家自然科學基金,、北京市自然科學基金、北京市卓越青年科學家項目,、中國博士后科學基金和國家資助博士后研究人員計劃的資助,。
論文鏈接:
https://pubs.acs.org/doi/10.1021/acs.jmedchem.4c02774
供稿:藥學院
編輯:李華山
封面圖設計:賀茂藤
審核:郭玲
