清華新聞網(wǎng)3月13日電 近年來,以PD-1/PD-L1(程序性死亡受體-1/程序性死亡配體-1)抗體為代表的免疫檢查點(diǎn)抑制劑(immune checkpoint inhibitors,ICIs)在腫瘤治療領(lǐng)域中取得了里程碑式的突破。然而,ICI療法在不同腫瘤患者中的效果差異很大,絕大部分的患者無法產(chǎn)生有效應(yīng)答,產(chǎn)生應(yīng)答的患者也很難長期獲益。如何克服ICI療法的局限性成為當(dāng)前腫瘤免疫研究領(lǐng)域的熱點(diǎn)問題。研究表明,腫瘤細(xì)胞內(nèi)在的免疫逃逸信號和具有免疫抑制性的腫瘤微環(huán)境都是阻礙ICI療法的關(guān)鍵因素。因此,要充分發(fā)揮ICI療法的臨床潛力,建立一個(gè)能同時(shí)抑制腫瘤細(xì)胞內(nèi)在免疫逃逸信號和降低腫瘤免疫微環(huán)境抑制性的新策略將成為重要思考方向。
3月12日,清華大學(xué)基礎(chǔ)醫(yī)學(xué)院鄭撼球課題組在《自然·癌癥》(Nature Cancer)上發(fā)表了題為“使用反義寡核苷酸同時(shí)靶向MALT1的死亡結(jié)構(gòu)域和副半胱天冬酶結(jié)構(gòu)域克服對免疫檢查點(diǎn)抑制劑的耐受性”(Targeting Both Death and Paracaspase Domains of MALT1 with Antisense Oligonucleotides Overcomes Resistance to Immune Checkpoint Inhibitors)的研究論文。
論文中,研究團(tuán)隊(duì)發(fā)現(xiàn)黏膜相關(guān)淋巴樣組織淋巴瘤易位蛋白(Mucosa-associated lymphoid tissue lymphoma translocation protein 1, MALT1)通過雙重機(jī)制促進(jìn)腫瘤免疫逃逸:一方面,MALT1通過蛋白酶活性上調(diào)PD-L1的表達(dá);另一方面,MALT1通過死亡結(jié)構(gòu)域促進(jìn)腫瘤相關(guān)巨噬細(xì)胞的M2型極化以增強(qiáng)腫瘤微環(huán)境的免疫抑制性。同時(shí),研究人員還通過反義寡核苷酸(antisense oligonucleotide, ASO)靶向MALT1,實(shí)現(xiàn)了對PD-L1的抑制和腫瘤微環(huán)境的重塑,克服了腫瘤對ICI療法的抵抗,充分體現(xiàn)了靶向MALT1在臨床應(yīng)用的治療前景。
首先,研究人員通過腫瘤細(xì)胞與CD8 T細(xì)胞共培養(yǎng)體系下的CRISPR-a篩選,鑒定出MALT1是導(dǎo)致腫瘤細(xì)胞抵抗CD8 T細(xì)胞殺傷的內(nèi)在免疫逃逸信號。隨后,通過小鼠腫瘤模型分析和單細(xì)胞測序技術(shù)等,研究人員發(fā)現(xiàn)MALT1還能介導(dǎo)腫瘤細(xì)胞促進(jìn)巨噬細(xì)胞的增殖和M2型極化,從而增強(qiáng)腫瘤微環(huán)境的免疫抑制性。
在機(jī)制上,MALT1一方面利用蛋白酶活性切割ROQUIN1和ROQUIN2,阻止它們降解PD-L1的mRNA,從而上調(diào)腫瘤細(xì)胞PD-L1的表達(dá),導(dǎo)致腫瘤細(xì)胞抵抗CD8 T細(xì)胞殺傷。另一方面,MALT1通過其死亡結(jié)構(gòu)域結(jié)合BCL10,參與腫瘤細(xì)胞中CARD-BCL10-MALT1(CBM)復(fù)合物的形成,激活NF-κB信號通路,促進(jìn)腫瘤細(xì)胞分泌CSF1、PGE2、CXCL1等因子。這些因子的分泌能促進(jìn)腫瘤相關(guān)巨噬細(xì)胞的增殖,并使它們極化為M2型巨噬細(xì)胞,加劇腫瘤微環(huán)境的免疫抑制性,促進(jìn)腫瘤免疫逃逸。
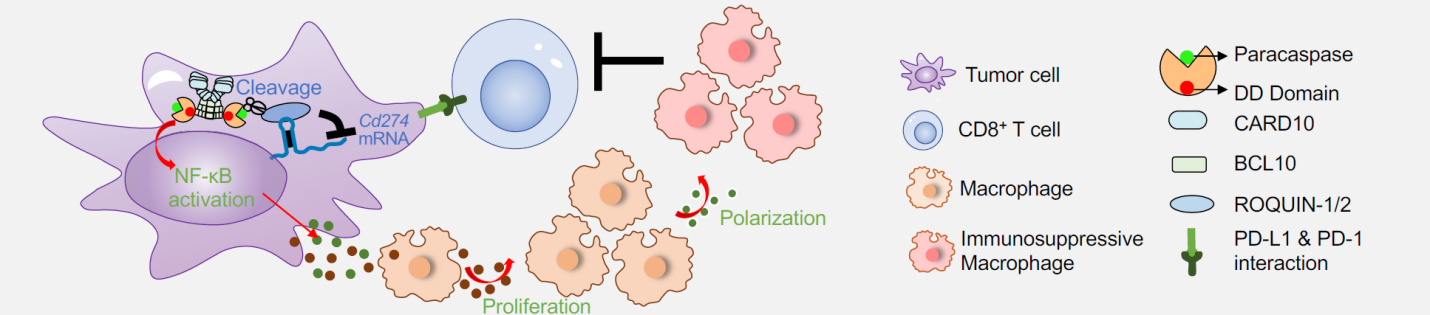
MALT1工作模式圖
由于MALT1通過兩種不同的機(jī)制促進(jìn)腫瘤免疫逃逸,靶向MALT1必須同時(shí)抑制其蛋白酶活性和死亡結(jié)構(gòu)域功能。然而,現(xiàn)有的MALT1抑制劑僅能抑制蛋白酶活性,并不能限制其死亡結(jié)構(gòu)域功能。因此,研究人員使用ASO技術(shù)靶向MALT1,在病人腫瘤樣本和臨床前小鼠腫瘤模型中成功抑制了MALT1的雙重作用。臨床前小鼠腫瘤模型研究還表明,通過ASO靶向MALT1能顯著減緩腫瘤的生長,提高ICI療法的響應(yīng)度和療效。
清華大學(xué)基礎(chǔ)醫(yī)學(xué)院、分子腫瘤學(xué)全國重點(diǎn)實(shí)驗(yàn)室、山西醫(yī)科大學(xué)-清華大學(xué)醫(yī)學(xué)院前沿醫(yī)學(xué)協(xié)同創(chuàng)新中心研究員鄭撼球?yàn)檎撐耐ㄓ嵶髡撸A(chǔ)醫(yī)學(xué)院2019級博士畢業(yè)生陶榆瑋為論文第一作者。清華大學(xué)基礎(chǔ)醫(yī)學(xué)院林欣教授團(tuán)隊(duì)和藍(lán)勛副教授團(tuán)隊(duì)、清華大學(xué)化學(xué)系喻國燦助理教授團(tuán)隊(duì)、中國醫(yī)學(xué)科學(xué)院腫瘤醫(yī)院周海濤教授團(tuán)隊(duì)和劉嘉琦副主任醫(yī)師團(tuán)隊(duì)為該研究提供了技術(shù)指導(dǎo)、數(shù)據(jù)分析、ASO系統(tǒng)遞送和病人樣本收集等幫助。研究得到國家自然科學(xué)基金、國家重點(diǎn)研發(fā)計(jì)劃等的支持。
論文鏈接:
https://www.nature.com/articles/s43018-025-00930-5
供稿:基礎(chǔ)醫(yī)學(xué)院
編輯:李華山
審核:郭玲
