清華新聞網(wǎng)3月20日電 細(xì)胞外蛋白(包括分泌蛋白與跨膜蛋白)在多細(xì)胞生物的生理調(diào)控中具有重要作用,其通過介導(dǎo)細(xì)胞間通訊協(xié)調(diào)復(fù)雜生理過程。病理狀態(tài)下,細(xì)胞外蛋白的異常表達(dá)或修飾與癌癥、神經(jīng)退行性疾病及心血管疾病等發(fā)生發(fā)展密切相關(guān)。值得注意的是,超過60%的FDA批準(zhǔn)藥物靶向細(xì)胞外蛋白,因此系統(tǒng)解析細(xì)胞外蛋白質(zhì)組對闡明生物過程分子機(jī)制、揭示疾病病理基礎(chǔ)及開發(fā)靶向治療策略具有重要意義。
近年來,盡管鄰近標(biāo)記酶(proximity labeling enzymes)和小分子光催化劑技術(shù)的發(fā)展促進(jìn)了細(xì)胞外蛋白質(zhì)組的解析,但這些方法的體內(nèi)應(yīng)用仍存在局限性。辣根過氧化物酶(Horseradish Peroxidase, HRP)的標(biāo)記依賴具有細(xì)胞毒性的過氧化氫(圖1a),限制了其在活體動(dòng)物中的直接使用;而生物素連接酶(如BioID和TurboID)雖然可以實(shí)現(xiàn)活體細(xì)胞內(nèi)蛋白的標(biāo)記,卻因細(xì)胞外微環(huán)境中ATP濃度不足導(dǎo)致胞外標(biāo)記效率受限。此外,內(nèi)源性生物素或過氧化氫均可能出現(xiàn)較高的背景干擾。可見光在活體組織中的穿透深度有限,光催化劑在體內(nèi)的應(yīng)用也面臨挑戰(zhàn)。
近日,清華大學(xué)藥學(xué)院秦為課題組研究開發(fā)了一種無毒的鄰近標(biāo)記技術(shù)TyroID,實(shí)現(xiàn)了活體內(nèi)細(xì)胞外蛋白質(zhì)組的高時(shí)空分辨率解析,該技術(shù)成功應(yīng)用于活體腫瘤異種移植模型HER2鄰近蛋白動(dòng)態(tài)解析、血漿蛋白代謝追蹤及小鼠海馬區(qū)特異性蛋白質(zhì)組標(biāo)記,解決了傳統(tǒng)鄰近標(biāo)記技術(shù)解析細(xì)胞外蛋白質(zhì)組的活體兼容性問題。
該研究發(fā)展了一種新型活體鄰近標(biāo)記技術(shù)TyroID(圖1b),用于實(shí)現(xiàn)細(xì)胞外蛋白質(zhì)組的時(shí)空動(dòng)態(tài)解析。TyroID 技術(shù)的核心是基于植物或細(xì)菌來源的酪氨酸酶(tyrosinase),其可以將生物正交的苯酚底物氧化為高反應(yīng)活性的鄰醌(o-quinone),特異性標(biāo)記鄰近蛋白中半胱氨酸、賴氨酸及組氨酸等親核氨基酸。與傳統(tǒng)鄰近標(biāo)記技術(shù)相比,TyroID無需依賴過氧化氫或可見光等外源激活條件,僅需添加酚類底物即可完成原位標(biāo)記。
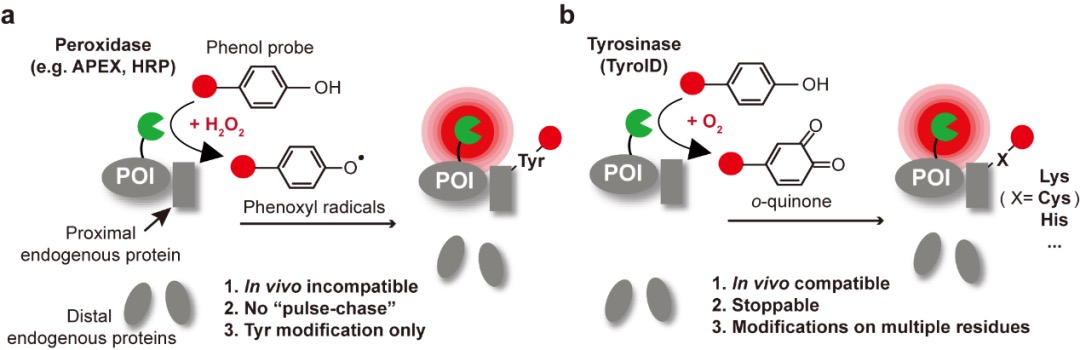
圖1.(a)過氧化物酶(如 APEX 和 HRP)標(biāo)記示意圖;(b)TyroID標(biāo)記示意圖
針對常規(guī)探針AP易滲入胞內(nèi)的缺陷,團(tuán)隊(duì)開發(fā)了膜非通透型探針“AxxP”——通過引入四聚乙二醇連接臂阻斷跨膜擴(kuò)散。實(shí)驗(yàn)證明,75nM abmTYR聯(lián)合50μM AxxP能在30分鐘內(nèi)實(shí)現(xiàn)乳腺癌細(xì)胞表面蛋白的特異性標(biāo)記,與膜標(biāo)志物GLUT1呈高度共定位,且維持生理狀態(tài)下的蛋白空間分布。基于二甲基化定量蛋白質(zhì)組學(xué),TyroID系統(tǒng)成功鑒定315個(gè)高置信度細(xì)胞外蛋白。通過super-TOPP-ABPP技術(shù)解析的修飾位點(diǎn)均位于蛋白胞外域,證明該方法具備解析跨膜蛋白拓?fù)浣Y(jié)構(gòu)的獨(dú)特能力。該研究進(jìn)一步將TyroID應(yīng)用于HER2受體鄰近蛋白組解析,通過抗體靶向策略識別出LGALS1、FUS等HER2互作蛋白,并經(jīng)Co-IP實(shí)驗(yàn)驗(yàn)證其結(jié)合強(qiáng)度與經(jīng)典互作蛋白TFRC相當(dāng)。
最后,基于TyroID無毒、快速標(biāo)記的優(yōu)勢,團(tuán)隊(duì)探索了其在活體中的應(yīng)用,這是基于過氧化物酶和可見光激活的鄰近標(biāo)記方法難以實(shí)現(xiàn)的。為此,研究人員設(shè)計(jì)了三項(xiàng)獨(dú)立的活體實(shí)驗(yàn),以驗(yàn)證TyroID在活體小鼠中應(yīng)用的有效性:第一,活體腫瘤中HER2鄰近蛋白的分析,鑒定出內(nèi)質(zhì)網(wǎng)ATP酶(VCP)、鈣調(diào)理蛋白2(CNN2)及分選連接蛋白9(SNX9)等在細(xì)胞培養(yǎng)實(shí)驗(yàn)中未發(fā)現(xiàn)的HER2鄰近蛋白;第二,定量分析44種血漿蛋白的turnover速率,揭示Apoc3、Apoa4和Apoe等載脂蛋白的高代謝特性;第三,海馬區(qū)原位標(biāo)記叢蛋白A1(Plxna1)、神經(jīng)軟骨蛋白(Ncdn)及神經(jīng)元膜糖蛋白M6-a(Gpm6a)等腦特異性蛋白。
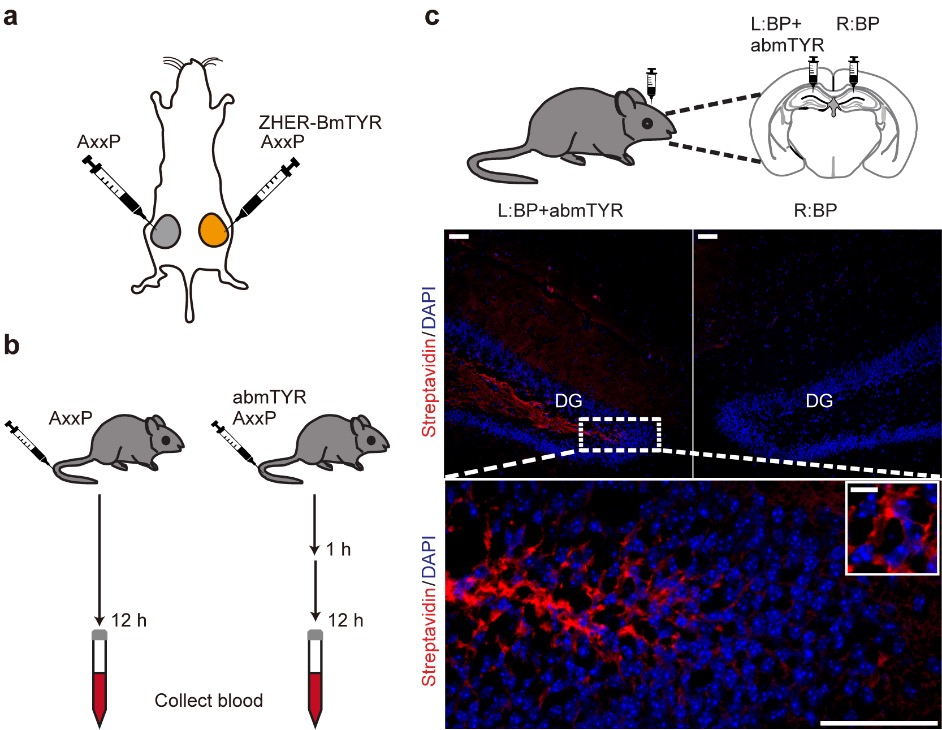
圖2.TyroID在活體內(nèi)的應(yīng)用
綜上,TyroID通過酶促生成鄰醌實(shí)現(xiàn)無毒、快速的細(xì)胞外標(biāo)記,突破了傳統(tǒng)技術(shù)對過氧化氫或可見光的依賴,為活體蛋白質(zhì)組動(dòng)態(tài)解析提供了創(chuàng)新工具。其在腫瘤微環(huán)境研究、血漿蛋白周轉(zhuǎn)監(jiān)測及神經(jīng)生物學(xué)領(lǐng)域的應(yīng)用,展現(xiàn)了廣闊的研究潛力。
相關(guān)研究成果以“活體兼容鄰近標(biāo)記技術(shù)TyroID解析細(xì)胞外蛋白質(zhì)組的時(shí)空動(dòng)態(tài)”(Spatiotemporally resolved mapping of extracellular proteomes via in vivo-compatible TyroID)為題,于3月15日發(fā)表于《自然·通訊》(Nature Communications)。
清華-北大生命科學(xué)聯(lián)合中心、清華大學(xué)藥學(xué)院助理教授秦為為論文的通訊作者,清華大學(xué)藥學(xué)院博士生張梓涓和博士后王妍坤為論文的第一作者。中國科學(xué)院遺傳與發(fā)育生物學(xué)研究所武照伐研究員為本文提供了重要實(shí)驗(yàn)幫助。
研究得到國家重點(diǎn)研發(fā)計(jì)劃青年科學(xué)家項(xiàng)目,國家自然科學(xué)基金重大研究計(jì)劃培育項(xiàng)目、面上項(xiàng)目,中國博士后面上項(xiàng)目,清華-北大生命科學(xué)聯(lián)合中心,清華大學(xué)篤實(shí)計(jì)劃,北京生物結(jié)構(gòu)前沿研究中心,北京分子科學(xué)國家實(shí)驗(yàn)室基礎(chǔ)研究基金,深圳市醫(yī)學(xué)研究基金等的支持。
論文鏈接:
https://www.nature.com/articles/s41467-025-57767-w
供稿:藥學(xué)院
編輯:李華山
審核:郭玲
