清華新聞網(wǎng)4月9日電 在生命科學(xué)領(lǐng)域,特別是在神經(jīng)科學(xué)、細(xì)胞生物學(xué)、病理學(xué)及發(fā)育生物學(xué)等子領(lǐng)域,隨著多項(xiàng)生物技術(shù)如基因編碼熒光探針、顯微技術(shù)和動(dòng)物遺傳學(xué)改造技術(shù)的革命,科學(xué)家們擁有了史無前例的實(shí)時(shí)、高精度、高保真測量跨時(shí)空分子活動(dòng)的科研手段,為進(jìn)一步揭示生命奧秘、造福人類奠定了堅(jiān)實(shí)的基礎(chǔ)。然而,這一強(qiáng)有力的先進(jìn)測量手段產(chǎn)生了海量并復(fù)雜的時(shí)空數(shù)據(jù),如何提取并刻畫其中的復(fù)雜時(shí)空模式(如異質(zhì)性空間分布和多向傳播),正成為制約科研突破的新瓶頸。傳統(tǒng)人工分析效率低下,現(xiàn)有分析技術(shù)與方法或因假設(shè)過于嚴(yán)苛而導(dǎo)致失真,或因計(jì)算效率不足難以應(yīng)對(duì)空間時(shí)間高維大數(shù)據(jù),亟需新的理論與手段。
清華大學(xué)自動(dòng)化系于國強(qiáng)教授課題組深耕該領(lǐng)域十余年,鉆研其中的基礎(chǔ)理論與核心技術(shù),近日終于有了突破性成果,于4月8日在國際頂尖雜志《細(xì)胞》(Cell)主刊上合作發(fā)表了題為“量化分析分子時(shí)空信號(hào)的快速、精準(zhǔn)、通用計(jì)算平臺(tái)”(Fast, accurate, and versatile data analysis platform for the quantification of molecular spatiotemporal signals)的研究論文,提出了時(shí)空統(tǒng)一的生物分子信號(hào)分析理論,并開發(fā)了基于該理論的開源智能計(jì)算平臺(tái)AQuA2。

圖1.AQuA2流程圖與主要技術(shù)創(chuàng)新
該成果的關(guān)鍵突破是提出了時(shí)空統(tǒng)一的理論框架,攻克了事件分解這一核心技術(shù),使得生命分子信號(hào)如鈣信號(hào)和多巴胺信號(hào)在時(shí)間和空間兩個(gè)不同的層面上得到統(tǒng)一的分析,無論是分子信號(hào)的空間變化還是時(shí)間上的動(dòng)態(tài)過程,都可以得到準(zhǔn)確靈活的檢測與量化。該成果的突破也依賴于近年來人工智能與機(jī)器學(xué)習(xí)技術(shù)的進(jìn)展。為了應(yīng)對(duì)低信噪比環(huán)境和更龐大的數(shù)據(jù)規(guī)模,AQuA2采用了包含概率統(tǒng)計(jì)理論與先進(jìn)機(jī)器學(xué)習(xí)算法在內(nèi)的策略。譬如,序統(tǒng)計(jì)理論被用來刻畫閾值操作帶來的統(tǒng)計(jì)偏差,從而提高低信噪比狀況下的魯棒性。研究團(tuán)隊(duì)開發(fā)了雙向推送線性組件操作算法(bidirectional pushing with linear component operations,BILCO)等先進(jìn)方法,使得AQuA2能夠在不犧牲精度的情況下顯著提高檢測效率,運(yùn)行速度提高約2倍,計(jì)算機(jī)內(nèi)存使用效率提高約10倍。AQuA2引入了共識(shí)功能單元(consensus functional unit,CFU)的概念來集成基于感興趣區(qū)域和基于事件的方法。如果一個(gè)空間區(qū)域產(chǎn)生重復(fù)的信號(hào)事件,它更有可能是一個(gè)功能單元,這種區(qū)域稱為CFU。CFU的提出,很好地結(jié)合了區(qū)域和事件定義,比感興趣區(qū)域提供了更大的靈活性,允許信號(hào)具有不同的大小、形狀和傳播模式,同時(shí)保持一致的空間基礎(chǔ)。這一改動(dòng)通過利用基于感興趣區(qū)域和基于事件的方法的優(yōu)勢,促進(jìn)更深層次的生物學(xué)見解。此外,引入CFU使得AQuA2能夠分析不同生物傳感器記錄的信號(hào)之間的相互作用。
值得一提的是,人工智能與機(jī)器學(xué)習(xí)技術(shù)的進(jìn)展促進(jìn)了前沿科研問題的有效解決,同時(shí),前沿科研問題也為先進(jìn)人工智能技術(shù)的發(fā)展提供了沃土,豐富了人工智能技術(shù)寶庫。例如,上文提到研究團(tuán)隊(duì)新開發(fā)的BILCO就為多時(shí)間序列匹配這一典型人工智能問題提供了新的技術(shù)方案。
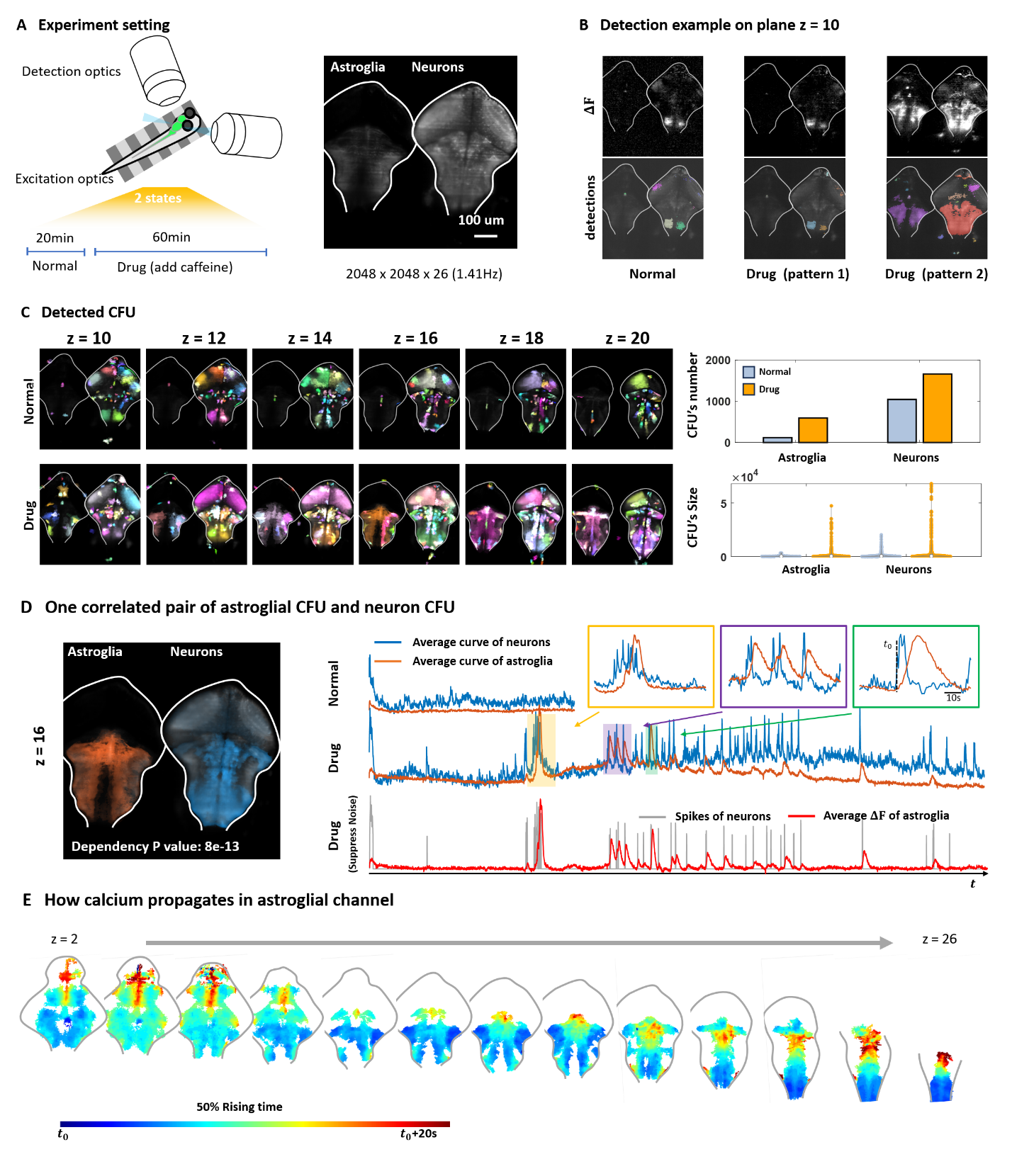
圖2.AQuA2識(shí)別咖啡因?qū)Π唏R魚星形膠質(zhì)細(xì)胞和神經(jīng)元信號(hào)模式的影響
研究團(tuán)隊(duì)利用AQuA2進(jìn)行了多項(xiàng)實(shí)驗(yàn),驗(yàn)證了其在復(fù)雜生物系統(tǒng)中的應(yīng)用價(jià)值。作為典型的發(fā)現(xiàn),研究團(tuán)隊(duì)展示了AQuA2如何識(shí)別神經(jīng)元和星形膠質(zhì)細(xì)胞之間的藥物依賴性相互作用,以及小鼠脊髓中不同的感覺運(yùn)動(dòng)信號(hào)傳播模式。
咖啡因作為中樞神經(jīng)系統(tǒng)興奮劑和腺苷受體阻滯劑/拮抗劑發(fā)揮作用,影響神經(jīng)元和神經(jīng)膠質(zhì)細(xì)胞的功能,并在一定程度上調(diào)節(jié)大腦的內(nèi)部環(huán)境。檢測結(jié)果顯示了兩種狀態(tài)下的代表性信號(hào)。在藥物狀態(tài)下,其中一種模式反映了正常狀態(tài),僅顯示神經(jīng)元信號(hào)。這種模式可能反映了由于游泳行為引起的信號(hào)激活。相反,在藥物狀態(tài)下的另一種模式顯示了星形膠質(zhì)細(xì)胞鈣信號(hào),通常伴隨著更大的神經(jīng)元信號(hào)。這種獨(dú)特的大腦活動(dòng)模式表明,由于咖啡因的加入,整個(gè)大腦的動(dòng)力學(xué)發(fā)生了變化。

圖3.AQuA2揭示感覺和運(yùn)動(dòng)誘發(fā)的星形膠質(zhì)細(xì)胞鈣信號(hào)在小鼠脊髓中的傳播差異
脊髓在傳遞感覺信息、協(xié)調(diào)運(yùn)動(dòng)和觸發(fā)反射動(dòng)作方面具有關(guān)鍵功能。在脊髓內(nèi),單個(gè)板層包含獨(dú)特的神經(jīng)元群體,表現(xiàn)出獨(dú)特的連接模式,并發(fā)揮專門的功能作用。AQuA2分析了小鼠脊髓中感覺誘發(fā)和運(yùn)動(dòng)誘發(fā)的星形膠質(zhì)細(xì)胞鈣信號(hào)傳播差異。研究結(jié)果表明,外周感覺刺激和運(yùn)動(dòng)動(dòng)作參與了不同脊髓板的神經(jīng)回路,這一發(fā)現(xiàn)對(duì)于星形膠質(zhì)細(xì)胞如何調(diào)節(jié)脊髓神經(jīng)回路活動(dòng)或可塑性具有重要意義。
AQuA2可以對(duì)多種信號(hào)進(jìn)行量化,既包括多種生物傳感器、細(xì)胞類型、器官、動(dòng)物模型的數(shù)據(jù),也包含不同顯微鏡技術(shù)和成像方法獲得的數(shù)據(jù),并且可以在分析的基礎(chǔ)上得到一定的生物學(xué)啟發(fā)。AQuA2提供了開源的MATLAB軟件包、Fiji插件和Web云服務(wù),能夠滿足開發(fā)和使用的需求。這些版本都配備了用戶友好的圖形界面,兼容處理二維、三維和雙色數(shù)據(jù),并且允許用戶結(jié)合生物學(xué)意義自定義參數(shù)。AQuA2的端到端特性將極大方便科學(xué)家們的實(shí)驗(yàn)分析過程,同時(shí)極大程度上保留了研究人員對(duì)算法進(jìn)行二次開發(fā)的可能性。
這一科研進(jìn)展不僅是提供了一個(gè)開源實(shí)用技術(shù)工具AQuA2,具有多應(yīng)用場景、高準(zhǔn)確度、高運(yùn)行效率、對(duì)用戶更加友好的特性。更重要的是,該成果為連接微觀分子活動(dòng)與宏觀生命現(xiàn)象的提供了重要的理論橋梁。它能夠很大程度上便利我們從生物分子的動(dòng)態(tài)變化的角度研究神經(jīng)系統(tǒng)、免疫反應(yīng)、代謝調(diào)控等重要生命過程,在時(shí)空范疇上對(duì)生命過程做一個(gè)更精準(zhǔn)深入的了解,為精準(zhǔn)醫(yī)療、智能藥物開發(fā)等臨床應(yīng)用提供關(guān)鍵技術(shù)支撐。
該研究由清華大學(xué)自動(dòng)化系于國強(qiáng)課題組,美國霍華德·休斯醫(yī)學(xué)研究所(HHMI Janelia)米沙·阿倫斯(Misha Ahrens)課題組,美國索爾克生物研究所(Salk Institute)阿克塞爾·尼默揚(yáng)(Axel Nimmerjahn)課題組,英國愛丁堡大學(xué)大衛(wèi)·萊昂斯(David A. Lyons)課題組,美國加州大學(xué)洛杉磯分校基拉·波斯坎澤(Kira E.Poskanzer)課題組,清華大學(xué)生命學(xué)院時(shí)松海課題組和復(fù)旦大學(xué)腦科學(xué)研究院鄧菡菲課題組共同合作完成。其中于國強(qiáng)為第一通訊作者,米沙·阿倫斯(Misha Ahrens)和阿克塞爾·尼默揚(yáng)(Axel Nimmerjahn)為共同通訊作者。研究得到國家自然科學(xué)基金的資助。
文章鏈接:
https://doi.org/10.1016/j.cell.2025.03.012
供稿:自動(dòng)化系
編輯:李華山
審核:郭玲
